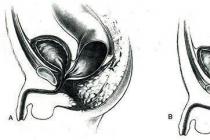
Hemija je nauka o sastavu, strukturi i svojstvima supstanci. Hemija proučava proces transformacije ovih supstanci, kao i zakone po kojima se te transformacije dešavaju.
Čovjek se počeo baviti hemijskom aktivnošću mnogo prije naše ere. To se dogodilo u vrijeme kada su ljudi naučili kako da dođu do metala. Tada počinje proizvodnja keramike, stakla, štavljenje kože, bojenje tkanina, stvaranje lijekova i proizvodnja kozmetike.
Još 300. godine prije Krista Egipćanin Zosima je stvorio enciklopediju koja se sastojala od 28 tomova. Ovi tomovi su prikupili znanje o međusobnim transformacijama supstanci u proteklih 500-600 godina.
Alhemija

Pojava alhemije se može smatrati početnim stadijem u razvoju hemije. Alhemija se zasnivala na idejama starogrčkih filozofa Empedokla, Platona i Aristotela o elementima prirode i njihovoj međusobnoj transformaciji. Verovalo se da postoje četiri principa: zemlja, voda, vazduh i vatra. I oni su u stanju da prelaze jedno u drugo, pošto je svako od njih jedno od stanja jedne primarne materije. A sve supstance nastaju kao rezultat kombinacije ovih početnih principa.
Alhemičari su transformisali jednu supstancu u drugu. Vjerovali su da i metali mogu proći kroz slične transformacije. Mnogi naučnici su bili zauzeti traženjem "kamena filozofa", koji je trebalo da pretvori obične metale u zlato. I tokom ovih pretraga u svojim laboratorijama, alhemičari su naučili kako da dobiju alkalije, mnoge soli, sumpornu i dušičnu kiselinu i etanol. Uz pomoć ovih supstanci mogli bi djelovati na druge tvari. Sredinom XIII veka evropski alhemičari su dobili barut.
Treba reći da je alhemija u Evropi bila zabranjena. I crkva i svjetovne vlasti zabranile su bavljenje alhemijom. Ali, uprkos tome, alhemija je bila popularna sve do početka XVI veka.
Razvoj hemije kao nauke

U 16. veku, irski naučnik Bojl oslobodio je hemiju od alhemije. On je sugerisao da su sve supstance sastavljene od hemijskih elemenata koji se ne mogu razložiti na jednostavnije delove. Možemo reći da je od tog vremena hemija postala posebna nauka.
Krajem 17. - početkom 18. vijeka, teorija njemačkog hemičara E.G. Stahl, objašnjavajući fenomene sagorevanja, oksidacije i redukcije metala. Ali ovu teoriju je sredinom 18. stoljeća prepoznao kao pogrešnu francuski fizičar Lavoisier, koji je ustanovio ulogu kisika u ovim procesima. M.V. Lomonosov je otkrio zakon održanja mase materije u hemijskim procesima.
Od kraja 18. veka do sredine 19. veka otkriven je čitav niz stehiometrijskih zakona koji su uspostavljali kvantitativne odnose (mase i zapremine) između reaktanata i produkta reakcije. Avogadrov zakon, zakoni održanja mase, ekvivalenti, konstantnost sastava, omjeri volumena, višestruki omjeri su zakoni na kojima se temelji stehiometrija. Ovi zakoni su omogućili stvaranje pravila za sastavljanje hemijskih jednačina i formula. Nakon eksperimentalne potvrde ovih zakona formirala se hemija kao nauka. Atomski i molekularni koncept strukture materije, potvrđen teorijom strukture hemijskih jedinjenja, koju je stvorio A.M. Butlerov. D.M. Mendeljejev je otkrio periodični zakon.
Nakon otkrića elektrona i radioaktivnosti krajem 19. vijeka, početkom 20. stoljeća razvijaju se teorija heteropolarnog (jonskog) veza i teorija homeopolarnog (kovalentnog) veza. Godine 1927. započeo je razvoj kvantnomehaničke teorije hemijskog vezivanja. Mendeljejevljeva doktrina o periodičnosti hemijskih elemenata je potvrđena. Postalo je moguće predvidjeti svojstva supstanci. Fizičke i matematičke metode su počele da se široko koriste za različite proračune u oblasti hemije. Pojavile su se nove fizičko-hemijske metode analize: elektronska i vibraciona spektrometrija, magnetohemija itd.
U dvadesetom veku, zahvaljujući dostignućima hemijske nauke, postalo je moguće dobiti supstance sa željenim svojstvima: sintetički antibiotici, sintetički polimeri, plastika, razni građevinski materijali, tkanine itd.
Savremena hemija blisko sarađuje sa drugim naukama. Kao rezultat toga, pojavile su se potpuno nove grane hemije: biohemija, geohemija, koloidna hemija, kristalohemija, elektrohemija, hemija makromolekularnih jedinjenja itd.
Važan pravac moderne hemije je proizvodnja jeftinog goriva, koje stvara alternativu glavnim modernim izvorima energije - nafti i gasu.
Precizni savremeni instrumenti i računari uveliko su pojednostavili istraživanja i matematičke proračune u oblasti hemije, povećali njihovu tačnost, brzinu i smanjili cenu.
apstraktno
Na temu: „Istorija razvoja neorganska hemija»
Apstraktni plan:
- Preduslovi za nastanak hemije kao nauke.
Hemija kao nauka nastala je u Drevni Egipat i koristio se uglavnom kao primijenjena nauka: za dobivanje bilo kakvih tvari i proizvoda s novim svojstvima koja su još uvijek bila nepoznata širokom krugu ljudi. Sveštenici starog Egipta koristili su svoje znanje o hemiji da bi dobili veštački nakit, balzamirali ljude, a takođe i da pokažu svoju moć prikazivanjem neke vrste hemijskog eksperimenta u javnosti. Nadalje, brojni eksperimenti počeli su pokušavati pretvoriti druge tvari u zlato, potraga za takozvanim "kamenom filozofa" koji bi to mogao učiniti.
2. Faze razvoja neorganske hemije.
U starom Egiptu, svećenici su briljantno posjedovaliprimenjena hemija, međutim, izdvojio je kao samostalnu oblast znanja. Hemija u starom Egiptu bila je dio "svete tajne umjetnosti" svećenika. Obrada i krivotvorenje dragog kamenja, balzamiranje leševa i druge, općenito, potpuno nemisteriozne operacije, bile su praćene molitvama i čarolijama. Egipćani su boga Ozirisa s glavom ptice smatrali zaštitnikom hemije. Znanje Egipćana u primijenjenoj hemiji pogodilo je Grke, a usvajajući njihova specifična znanja, Grci su preuzeli mnogo misticizma.
Prvi značajniji predstavnik grčko-egipatske hemije, čije je ime došlo do nas, bio je Bolos od Mendea (oko 200. godine p.n.e.), grada u delti Nila. U svojim spisima, Bolos je koristio ime Demokrit i stoga se naziva "Bolos-Democritus" ili ponekad "Pseudo-Democritus". Bolos se posvetio jednom od najvažnijih zadataka kemije - transformaciji jednog metala u drugi, a posebno transformaciji olova ili željeza u zlato ( transmutacija).
Prema teorije o četiri elementa, različite supstance na Zemlji razlikuju se samo po prirodi kombinacije elemenata. Ova hipoteza bi se mogla prihvatiti bez obzira na atomističke poglede, budući da se elementi mogu miješati i kao atomi i kao homogene supstance. Zaista, pretpostavka da su sami elementi međusobno zamjenjivi nije bila neosnovana. Moglo bi se pretpostaviti da se voda, prilikom isparavanja, pretvara u vazduh, koji se zauzvrat pretvara u vodu tokom kiše. Drvo, kada se zagrije, pretvara se u vatru i dim (vrsta zraka) itd.
Zašto, u ovom slučaju, ne dozvoliti mogućnost bilo kakve promjene? Možda sve zavisi od izbora metode? Crvenkasti kamen može se pretvoriti u sivo željezo uz pomoć brojnih trikova. Međutim, u vrijeme Ahileja, najhrabrijeg od starogrčkih heroja, ove tehnike su bile nepoznate, pa je Ahil bio primoran da opsjeda Troju, obučen u bronzani oklop. Zašto je nemoguće, nekim drugim metodama, nepoznatim u doba Aleksandra Velikog, sivo gvožđe pretvoriti u žuto zlato?
Bolos je u svojim radovima dao detaljne opise metoda za dobijanje zlata, ali to nije bila prevara. Možete, na primjer, legirati bakar sa metalnim cinkom i dobiti mesing - leguru žuta boja, odnosno boje zlata. Vrlo je vjerovatno da je za drevne istraživače proizvodnja metala zlatne boje značila proizvodnju samog zlata.
U 7. veku Arapi su se pojavili na svjetskoj sceni. Do tada su živeli izolovano u pustinjama Arapskog poluostrva, ali su od druge polovine prvog milenijuma, pod zastavom nove religije – islama, krenuli u pobednički pohod i zauzeli velika područja zapadne Azije i severne Afrike. . Godine 641. AD e. napali su Egipat i ubrzo okupirali cijelu zemlju, a nekoliko godina kasnije ista je sudbina zadesila Perziju. Nastalo je ogromno arapsko carstvo. Imitirajući drevne vladare, arapski halife su počeli da pokroviteljuju nauke, a u VIII-IX vijeku. pojavili su se prvi arapski hemičari. Arapi su transformisali riječ "hemija" u "al-hemiju". Evropljani su kasnije ovu riječ posudili od Arapa, i kao rezultat toga, izrazi "alkemija" i "alhemičar" pojavili su se u evropskim jezicima. Termin "alhemija" danas se koristi kada se govori o periodu istorije hemije, koji obuhvata oko dve hiljade godina, od 300. do 1600. godine.
Po prvi put, Arapi su se susreli s hemijom na prilično neobičan način. Godine 670. brodovi arapske flote koji su opsjedali Carigrad (najveći i najmoćniji grad u kršćanskom svijetu) spaljeni su "grčkom vatrom" - hemijskom smjesom koja, kada izgori, stvara jak plamen koji se ne može ugasiti vodom. Prema legendi, ovu mješavinu je napravio hemičar Kallinikos, koji je pobjegao iz svog rodnog Egipta (ili možda Sirije), bježeći od Arapa.
Stranice evropske istorije hemije iz perioda između 300. i 1100. godine. zapravo prazan. Nakon 650. godine razvoj grčko-egipatske alhemije potpuno su kontrolisali Arapi i to se nastavilo pet stoljeća. Tragovi ovog perioda sačuvani su u nizu hemijskih izraza sa arapskim korenima: alembik (alembik), alkalija (alkalija), alkohol (alkohol), carboy (pletena boca), nafta (ligroin), cirkon (cirkonijum) itd.
Najtalentovaniji i najpoznatiji arapski alhemičar bio je Jabir ibn Hayyan (721-815), koji je kasnije postao poznat u Evropi pod imenom Geber. Živio je na vrhuncu Arapskog carstva (pod Harunom al-Rašidom, slavljen u Hiljadu i jednoj noći). Brojna Jabirova djela napisana su na prilično razumljivom jeziku. (Mnoge od knjiga koje mu se pripisuju, međutim, možda su kasnije napisali drugi alhemičari.) Džabir je opisao amonijak i pokazao kako se pravi bijelo olovo. Destilirao je sirće da bi dobio sirćetnu kiselinu, najjaču kiselinu poznatu u to vrijeme. Uspio je dobiti slabu otopinu dušične kiseline.
Džabir je proučavao mogućnost transmutacije metala, a ove njegove studije imale su snažan utjecaj na sljedeće generacije alhemičara. Džabir je vjerovao da je živa poseban metal jer je zbog svog tečnog oblika sadržavala vrlo malo nečistoća. Sumpor ima ista neobična svojstva: može se zapaliti (a osim toga, žut je, poput zlata). Džabir je vjerovao da je svih ostalih sedam metala nastalo iz mješavine žive i sumpora, koji "sazrevaju" u utrobi zemlje. Zlato, najsavršeniji metal, najteže se formira. Stoga, da bi se dobilo zlato, potrebno je pronaći supstancu koja ubrzava "sazrijevanje" zlata. U drevnim legendama se govorilo da je ova supstanca suvi prah. Grci su ga zvali xerion, ili "suh", Arapi su ga promijenili u al-iksir, i na kraju se riječ eliksir pojavila u evropskim jezicima. U Evropi je ova nevjerovatna supstanca nazvana kamenom filozofom. (Podsjetimo se da su prije 1800. svi "naučnici" bili nazivani "filozofima".) Eliksir je trebao imati i druga čudesna svojstva: da liječi sve bolesti i, što je najvažnije, daje besmrtnost. I u narednim stoljećima alhemičari su slijedili dva paralelna puta: jedni su tražili zlato, drugi - eliksir života, koji je davao besmrtnost.
Još jedan arapski alhemičar Ar-Razi (865-925), koji je u Evropi postao poznat pod imenom Rhazes, bavio se medicinom i alhemijom. Osvojio je skoro istu slavu kao i Džabir. Ar-Razi je opisao način pripreme gipsa i način postavljanja gipsanog zavoja za fiksiranje slomljene kosti. Proučavao je i opisao metalni antimon. Džabir je smatrao sumpor principom zapaljivosti, živu principom metalnosti, Ar-Razi je dodao na ova dva principa treći - princip tvrdoće, odnosno soli. Isparljiva živa i zapaljivi sumpor formirali su čvrste materije samo u prisustvu treće komponente, soli.
Ar-Razi se više zanimao za medicinu od Džabira, ali najpoznatiji ljekar je bio Ibn-Sina (oko 980-1037), iz Buhare, mnogo poznatiji pod latiniziranim imenom Avicena. Njegovi spisi su služili kao najvažniji vodič za lekare tokom mnogih vekova. Avicena je bio jedini alhemičar koji nije vjerovao u mogućnost dobivanja zlata iz drugih metala. Avicena je bio posljednji veliki učenjak arapskog svijeta; bilo je vrijeme za pad. Razorni napadi mongolskih hordi ubrzali su ovaj proces. Centar naučne misli ponovo se preselio u Evropu. Godine 1096. započeo je prvi krstaški rat; Kršćani su počeli da osvajaju zemlje koje su zauzeli od muslimana. Godine 1099. kršćani su osvojili Jerusalim. Gotovo dva stoljeća na obali Sirije postojala je kršćanska država. Došlo je do određenog miješanja kultura, a šačica kršćana koji su se vratili u Evropu upoznali su Evropljane sa dostignućima arapske nauke. Istovremeno, hrišćani su postepeno povratili Španiju, koju su Arapi zauzeli početkom 8. veka. Tokom ovih ratova, hrišćanska Evropa je saznala za briljantnu mavarsku civilizaciju. Evropljani su saznali da su Arapi vlasnici knjižnog blaga: djela grčkih učenjaka koje su prevodili, poput Aristotela, i spisa njihovih vlastitih učenjaka, poput Avicene. Unatoč otporu Arapa, koji nisu htjeli prenijeti tako vrijedna djela svom zakletom smrtnom neprijatelju, počeli su pokušaji da se ta djela prevedu na latinski. Francuski naučnik Herbert (oko 940-1003), koji je 999. postao papa Silvester II, na sve načine je doprineo ovom poduhvatu. Engleski učenjak Robert od Chestera bio je među onima koji su prvi preveli (oko 1144.) arapska djela o alhemiji na latinski. Našao je mnogo sljedbenika. Najbolji prevodilac bio je Italijan Gerard od Kremone (oko 1114-1187). Većinu svog života proveo je u španskom gradu Toledu, koji su hrišćani ponovo zauzeli 1085. godine, i preveo je 92 traktata sa arapskog. Počevši od 1200. godine, evropski naučnici su mogli, pošto su se pobliže upoznali sa nasleđem alhemičara prošlosti, ponovo pokušati da krenu napred trnovitim putem znanja. Prvi istaknuti evropski alhemičar bio je Albert od Bolsteda (oko 1193-1280), poznatiji kao Albertus Magnus (Albert Veliki). Pažljivo je proučavao Aristotelova djela i zahvaljujući njemu Aristotelova filozofija je dobila poseban značaj za naučnike kasnog srednjeg vijeka i početka novog vijeka. Albert Veliki, opisujući svoje alhemijske eksperimente, tako precizno karakteriše arsen da mu se ponekad pripisuje otkriće ove supstance, iako je, barem u nečistoćama, arsen bio poznat alhemičarima pre njega. Savremenik Albertusa Magnusa bio je engleski učeni monah Rodžer Bekon (1214-1292), koji je danas najpoznatiji po svom jasno izraženom uverenju da je ključ napretka nauke eksperimentalni rad i primena matematičkih metoda na njega. Bio je u pravu, ali svijet još nije bio spreman za to. Bekon je pokušao da napiše univerzalnu enciklopediju znanja iu svojim spisima dao je prvi opis baruta. Ponekad ga nazivaju izumiteljem baruta, ali to nije istina: pravi pronalazač je ostao nepoznat. Izumom baruta srednjovjekovni dvorci prestali su biti neosvojiva uporišta, a pješački ratnik postao je opasniji od konjanika obučenog u oklop.
Radovi srednjovekovnih alhemičara - španskog lekara Arnalda od Villanove (oko 1240-1311) i Rejmonda Lula (1235-1313), Bekonovih savremenika, prožeti su mističnim duhom alhemije (iako je sumnjivo da su oni zapravo bili autori ovih radova). Ovi radovi su uglavnom posvećeni transmutaciji. Vjerovalo se da je Lully čak proizvodio zlato za rasipnog kralja Engleske, Edwarda II. Ime najistaknutijeg srednjovekovnog alhemičara ostaje nepoznato; svoje radove potpisivao je imenom Džabir, arapski alhemičar koji je živio šest stoljeća prije njega. Ovaj "Pseudo-Jabir" je vjerovatno bio Španac i živio je u 14. vijeku. Pseudo-Jabir je prvi opisao sumporna kiselina- jedan od mnogih važnih jedinjenja današnja hemija (posle vode, vazduha, uglja i nafte). Također je opisao kako nastaje jaka dušična kiselina. Sumporna i jaka azotna kiselina dobijale su se iz minerala, dok su se sve dosad poznate kiseline, poput sirćetne kiseline, dobijale iz supstanci biljnog ili životinjskog porekla.
Otkriće jakih mineralnih kiselina bilo je najvažnije dostignuće u hemiji od uspješnog vađenja željeza iz rude oko 3000 godina ranije. Koristeći jake mineralne kiseline, evropski hemičari su bili u stanju da izvedu mnoge nove reakcije i uspeli su da rastvore supstance koje su stari Grci i Arapi smatrali nerastvorljivim (među Grcima i Arapima sirćetna kiselina je bila najjača kiselina).
Mineralne kiseline dale su čovječanstvu mnogo više nego što bi zlato moglo dati da se naučilo da se dobije transmutacijom. Kada bi zlato prestalo da bude rijedak metal, odmah bi depresiralo. Vrijednost mineralnih kiselina je veća, što su jeftinije i pristupačnije. Ali, nažalost, takva je ljudska priroda - otkriće mineralnih kiselina nije impresioniralo, a potraga za zlatom se nastavila.
Vrijeme je prolazilo, a alhemija je, nakon obećavajućeg početka, po treći put počela degenerirati (prvi put među Grcima, drugi put - među Arapima). Potraga za zlatom postala je djelo mnogih prevaranta, iako velikih naučnika čak iu prosvijećenom XVII vijeku. (na primjer, Boyle i Newton) nisu mogli odoljeti iskušenju da pokušaju uspjeti na ovom polju.
I opet, kao pod Dioklecijanom, proučavanje alhemije je bilo zabranjeno. Zabrana je imala dva cilja: bilo je nemoguće dozvoliti deprecijaciju zlata (odjednom transmutacija uspeva!) I bilo je potrebno boriti se protiv prevare. Godine 1317. papa Jovan XXII je anatemisao alhemiju, a pošteni alhemičari, primorani da kriju šta rade, postali su još zagonetniji, iako su alhemijske prevare cvetale kao i ranije. Međutim, vjetrovi promjena u Evropi su već bjesnili. Istočno rimsko (ili Vizantijsko) carstvo je opstalo zadnji dani. Godine 1204. prijestolnicu carstva, Konstantinopolj, varvarski su opljačkali krstaši, a većina spomenika grčke kulture koji su preživjeli do tog vremena potpuno je uništena. Godine 1261. Grci su vratili grad, ali od njegovog nekadašnjeg sjaja nije sačuvan ni trag. U naredna dva veka trupe turskih osvajača neumitno su se približavale gradu, a 1453. godine Carigrad je pao i zauvek postao turski. Bježeći od najezde Turaka, grčki naučnici su pobjegli u Evropu, a znanja, tradicije starogrčke nauke koje su ponijeli sa sobom imalo je snažan podsticaj. U Evropi je započeo period mukotrpnog istraživanja i važnih otkrića.
U XIII veku. Izumljen je magnetni kompas i počela se razvijati navigacija. Prvo je proučavana obala Afrike, a 1497. godine obavljeno je putovanje oko ovog kontinenta. Evropa je počela direktno trgovati sa Indijom i drugim zemljama u regionu, ne pribjegavajući posredovanju muslimanskih zemalja. Još su impresivnija bila putovanja Kristofora Kolumba (1492-1504), zahvaljujući kojima je (iako sam Kolumbo to nikada nije priznao) otkrivena druga polovica svijeta. Evropljani su naučili toliko toga što nije bilo poznato velikim grčkim filozofima da se imao osjećaj da su Grci ipak obični ljudi koji, kao i svi ljudi, mogu pogriješiti, pa stoga nije potrebno uzimati sve njihove izjave. na vjeru. Evropljani su dokazali svoju superiornost u plovidbi, pa se moglo pokušati nadmašiti ih i u drugim naukama.
U istom „dobu otkrića“, njemački pronalazač Johannes Gutenberg (oko 1397-1468) izumio je prvu štampariju sa pokretnim pismom, sakupljajući koju je bilo koja knjiga mogla biti odštampana u tekst. Po prvi put u istoriji postalo je moguće proizvoditi knjige jeftino i u dovoljnim količinama. Jedna od prvih objavljenih je pjesma Lukrecija, zahvaljujući kojoj je atomistička doktrina bila široko rasprostranjena u Europi. Sa pronalaskom štamparstva, nepopularni pogledi nisu nestali samo zato što se niko nije želeo truditi da prepisuje takve knjige.
Godine 1543. objavljene su dvije knjige čiji su autori iznosili stavove vrlo hrabre za ono doba. Autor jedne od ovih knjiga bio je poljski astronom Nikola Kopernik (1473-1543), koji je tvrdio da centar svemira nije Zemlja, kako su vjerovali drevni astronomi, već Sunce. Autor druge knjige, flamanski anatom Andrej Vesalius (1514-1564), opisao je ljudsku anatomiju sa neviđenom tačnošću. Rad Vesaliusa, zasnovan na ličnim zapažanjima, opovrgnuo je mnoge ideje koje sežu do starogrčkih izvora.
Ovo istovremeno rušenje grčke astronomije i medicine (iako su grčke ideje još uvijek dominirale na nekim mjestima stoljeće ili više) označilo je početak naučna revolucija, koji je vrlo sporo prodirao u svijet alhemije, manifestirajući se uglavnom u mineralogiji i medicini.
Potpuno drugačije razumijevanje problema hemije ocrtano je u djelima dvojice savremenika doktora - Nijemca Georga Bauera (1494-1555) i Švajcarca Teofrasta Bombasta von Hohenheima (1493-1541). Bauera, poznatijeg pod imenom Agricola (što na latinskom znači "seljak"), zanimala je mineralogija i njena moguća povezanost s medicinom. Pokušaji otkrivanja takve veze (kao i kombinacija doktora i mineraloga) općenito su karakteristični za hemiju tog perioda i naredna dva i po stoljeća. U svojoj knjizi "O metalurgiji" ("De Re Metallica"), objavljenoj 1556. godine, Agrikola je sistematizovao praktično znanje koje je stekao od savremenih rudara. Ova knjiga, napisana jednostavnim jezikom, sa prekrasnim ilustracijama rudarskih uređaja, odmah je postala popularna i smatra se klasičnim djelom našeg vremena. Ovo je najznačajnije djelo o hemijskom inženjerstvu koje se pojavilo prije 1700. godine; od svog objavljivanja, mineralogija je priznata kao nauka. (Najvrednijom knjigom o metalurgiji i opštoj primenjenoj hemiji pre Agrikole smatralo se da je delo monaha Teofila, najverovatnije Grka koji je živeo oko 10. veka.)
Von Hohenheim je ušao u istoriju pod imenom Paracelsus, koji je sam izabrao, odnosno "superiorni od Celza". Celsus je drevni rimski naučnik koji je pisao o medicini. Njegovi spisi, neposredno pre štampanja, ispostavili su se (zahvaljujući Paracelzusu) predmetom prekomernog i nerazumnog obožavanja. Paracelsus je, poput Avicene, vjerovao da glavni zadatak alhemije nije traženje načina za dobivanje zlata, već proizvodnja lijekova. Prije Paracelsusa, biljni preparati su se koristili kao takvi, ali je Paracelsus čvrsto vjerovao u djelotvornost lijekova napravljenih od minerala. Uprkos njegovom negativan stav Za ideju transmutacije, Paracelsus je bio alhemičar stare škole. Prihvatio je starogrčku doktrinu o četiri elementa-elementa i doktrinu Arapa o tri elementa-principa (živa, sumpor i so), tražio je eliksir života (i čak je tvrdio da ga je pronašao). Paracelsus je bio siguran da je otkrio metalni cink, a ponekad mu se zapravo pripisuje čast ovog otkrića, iako je cink u sastavu rude i u leguri sa bakrom (mesing) bio poznat još u antici. Paracelsusovi spisi izazvali su kontroverze čak i pola veka nakon njegove smrti. Paracelsovi sljedbenici su pojačali mistični sadržaj pogleda svog učitelja i neke od njih sveli na praznovjerje, i to u vrijeme kada su alhemičari počeli težiti konkretnosti i racionalizmu!
Njemački doktor alhemičar Andrei Liebau (oko 1540-1616), poznat pod latiniziranim imenom Libava, objavio je 1597. godine "Alhemiju" - prvi udžbenik hemije u istoriji. Libavy je prvi opisao pripremu hlorovodonične kiseline, kalajnog tetrahlorida, amonijum sulfata i "aquaregia" (aquaregia) - mešavine azotne i hlorovodonične kiseline, koja je dobila ime zbog svoje sposobnosti da rastvara zlato. Libavy je vjerovao da se mineralne tvari mogu identificirati po obliku kristala dobivenih nakon isparavanja otopine. Ipak, bio je siguran da je transformacija metala u zlato moguća i da će otkriće metode za proizvodnju zlata biti kruna hemijske nauke, iako se složio sa Paracelzusom da je glavni zadatak alhemije da služi medicini. U svom radu, napisanom jasnim, jasnim jezikom, Libavy je žestoko napadao nejasne teorije, koje je nazvao "paracelsijskim". Njemački izdavač Johann Tölde objavio je 1604. godine knjigu izvjesnog srednjovjekovnog monaha Vasilija Valentina (najvjerovatnije je to bio pseudonim samog Töldea) pod naslovom Antimonove trijumfalne kočije, koja je postala nadaleko poznata. Najistaknutiji predstavnik novog pravca u hemiji bio je njemački hemičar Johann Rudolf Glauber (1604-1668). Po obrazovanju doktor, bavio se razvojem i usavršavanjem metoda za dobijanje raznih hemikalija. Glauber je razvio metodu za proizvodnju hlorovodonične kiseline reakcijom sumporne kiseline sa običnom solju. Nakon pažljivog proučavanja ostatka dobivenog nakon destilacije kiselina (natrijum sulfata), Glauber je otkrio da ova tvar ima snažno laksativno djelovanje. Ovu supstancu je nazvao "nevjerovatna sol" (sal mirabile) i smatrao je lijekom za liječenje, gotovo eliksirom života. Glauberovi suvremenici su ovu sol nazivali Glauberovom, a ovo ime se održalo do danas. Glauber se bavio proizvodnjom ove soli i niza drugih, po njegovom mišljenju, vrijednih lijekova i postigao uspjeh u ovoj oblasti. Glauberov život je bio manje bogat događajima od života njegovih savremenika koji su tražili načine da dođu do zlata, ali je bio prosperitetniji. Čak i oni koji su bili gluvi na naučne argumente nisu mogli a da ne budu pod uticajem stvarnog života. Nauka o mineralima i medicini u razvoju pokazala se toliko primamljivom i profitabilnom da nije imalo smisla gubiti vrijeme na beskrajne neuspješne pokušaje da se dođe do zlata. Zaista, u sedamnaestom veku značaj alhemije je stalno opadao, a u XVIII veku. postepeno je postalo ono što danas nazivamo hemijom.
- Doprinos ruskih naučnika razvoju neorganske hemije.
Počeci domaće hemijske nauke datiraju iz 18. veka, kada je osnovana Sankt Peterburška akademija nauka. Prema planu Petra I, akademija je trebala ispuniti dva glavna zadatka: „proizvoditi i izvoditi nauke“ i „da ih širi među ljudima“. Za to je, prije svega, bilo potrebno obučiti kadrove ruskih naučnika u različitim oblastima znanja i privući strane naučnike da proučavaju prirodne resurse Rusije.
Od prvih godina postojanja Akademije nauka svi su bili povezani s njom. naučna dostignuća u Rusiji. Takvi poznati naučnici kao što su Johann i Daniel Bernoulli, L. Euler, S.P. Krašenjinjikov, P.S. Pallas, I.I. Lepekhin, N.Ya. Ozeretskovsky, Ya.D. Zakharov i drugi.
Studij hemije na Akademiji nauka započeo je 1731. godine izborom Johanna Georga Gmelina (17091755) za akademika. Gmelin je vlasnik prvog hemijskog istraživanja, objavljenog u "Proceedings of the St. Petersburg Academy of Sciences", članak "O povećanju težine određenih tijela tokom pucanja".
Tokom XVIII veka. Johann Gottlob Lehmann (17191767), Erik Gustav (Kiril Gustavovič) Laxman (17371796), Tobias Johann (Tovy Yegorovich) Lovitz (17571804), Vasilij Mihajlovič Severgin (17651826), Appolos Musin (17651826), Appolos Musin,18Pholos i drugi. Glavna dostignuća ovog veka u oblasti hemije vezuju se za ime Mihaila Vasiljeviča Lomonosova (17111765). Iako se Lomonosov, zbog izuzetno višestruke prirode svog stvaralačkog (matematika, fizika, hemija, nauke o Zemlji, astronomija) i obrazovne delatnosti, s pravom naziva enciklopedijskim naučnikom, njegova primarna pažnja bila je usmerena na razvoj fizike i hemije. Osnovna aktivnost naučnika u oblasti hemije je želja da se ova potonja potkrepi kao nauka zasnovana na savezu sa matematikom, mehanikom i fizikom. Osnovna dostignuća Lomonosova uključuju sledeće: skrenuo je pažnju (1756) na fundamentalni značaj zakona održanja mase materije u hemijskim reakcijama; ocrtao (17411750) temelje svoje korpuskularne (atomsko-molekularne) doktrine, koja je razvijena tek jedan vek kasnije; izneo (17441748) kinetičku teoriju toplote; obrazložio (1747-1752) potrebu uključivanja fizike u objašnjavanje hemijskih pojava i predložio naziv "fizička hemija" za teorijski deo hemije, a "tehnička hemija" za praktični deo. Lomonosov je prvi pročitao "Kurs prave fizičke hemije" na Sankt Peterburškoj akademiji nauka. 1748. godine, na inicijativu naučnika, izgrađena je prva hemijska laboratorija u Rusiji, namenjena za naučne i obrazovne svrhe. Za ovu laboratoriju razvio je širok istraživački program, čija je središnja tačka bila proučavanje onih pojava koje se javljaju u mješovitom tijelu tokom kemijske interakcije. U periodu 17481757. Radovi naučnika uglavnom su bili posvećeni rešavanju teorijskih i eksperimentalnih problema hemije. Provodeći eksperimente sa pečenjem metala u zatvorenim posudama, pokazao je (1756) da se njihova težina ne mijenja nakon zagrijavanja i da je mišljenje R. Boylea o dodavanju toplinske tvari metalima pogrešno; proučavane tečne, gasovite i čvrsto stanje tijela; prilično precizno utvrđeni koeficijenti ekspanzije plinova; proučavao rastvorljivost soli na različitim temperaturama; proučavao uticaj električne struje na rastvore soli, utvrdio činjenice o smanjenju temperature tokom rastvaranja soli i smanjenju tačke smrzavanja rastvora u poređenju sa čistim otapalom; ustanovio razliku između procesa rastvaranja metala u kiselini, praćenog hemijskim promenama, i procesa rastvaranja soli u vodi, koji se odvija bez hemijskih promena u otopljenim materijama. Lomonosov posjeduje veliki broj praktičnih istraživanja. Bio je tvorac mnogih hemijskih industrija (anorganski pigmenti, glazure, staklo, porcelan); razvio tehnologiju i formulaciju stakla u boji, koje je koristio za izradu mozaičkih slika; izmislio porcelan. Bavio se analizom ruda, soli i drugih proizvoda; opisao procese dobivanja željeznog sulfata, bakra iz bakar sulfata, sumpora iz sumpornih ruda, stipse, sumporne, dušične i klorovodične kiseline. Lomonosovljevo djelo "Prvi temelji metalurgije ili rudarstva" (1763.), u kojem je razmatrao svojstva različitih metala, dao njihovu klasifikaciju i opisao metode dobijanja, ne samo da je postavio prve blokove u temelje ruskog hemijskog jezika, ali i postavio temelje za sistematski rad narednih naučnika.generacija na istraživanju i razvoju prirodnih resursa Rusije. Tradicije M.V. Lomonosova, vezano za proučavanje ruda i minerala u Rusiji, nastavljene su u drugoj polovini 18. i početkom 19. veka, kada su sprovedene brojne primenjene hemijske studije. Od posebnog značaja u ovom periodu bila je obrazovna aktivnost ruskih hemičara. I.G. Leman, koji je preuzeo nakon M.V. Lomonosov, Odeljenje za hemiju Sankt Peterburgske akademije nauka i preuzeo je hemijsku laboratoriju, proučavao sibirsku olovnu rudu krokoita, opisao ruske minerale koji sadrže volfram i hrom, objavio (1772.) priručnike o mineralogiji i ispitivanju umetnosti prevedene na ruski . Npr. Laxman je proučavao rudna bogatstva Altaja i istočnog Sibira. Kao neumoljivi protivnik spaljivanja šumskih površina u cilju akumulacije pepela, koji je bio neophodan za dobijanje potaše kao glavne sirovine u proizvodnji stakla, Laxman je razvio novu bezkalijsku metodu za pravljenje stakla na bazi prirodne glauberove soli (natrijum sulfat dekahidrata). ). Takođe je predložio (1769) metodu za dobijanje kuhinjske soli iz slane vode slanih jezera smrzavanjem i isparavanjem; razvio tehnologiju salitre, sode i stipse. Tokom celog 18. veka razvoj hemijskog znanja dobio je efektivnu podršku rukovodstva Akademije nauka, bilo da je to bio njen prvi predsednik L.L. Blumentrost (17251733) ili prva žena redateljica E.R. Daškov (17831796). U periodu kasnog 18. i početka 19. veka najveći doprinos razvoju hemijske nauke dali su akademici V.M. Severgin i T.E. Lovitz. V.M. Severgin od 1793. akademik (profesor) Petrogradske akademije nauka. Godine 1805-1826 kao priznanje za visoke naučne zasluge, šest puta zaredom biran je za člana Odbora Akademije. Glavni Severginovi naučni radovi posvećeni su opštoj i neorganskoj hemiji. Razvio je hemijski pravac u mineralogiji, smatrajući proučavanje sastava i strukture minerala glavnim zadatkom ove nauke; prvi je formulisao koncept parageneze („susjednost minerala“); stajao je na početku kolorimetrijske analize; predložio (1795) metodu kvantitativnog određivanja zasnovanu na poređenju intenziteta boje rastvora. Severgin je bio autor prvih ruskih priručnika o hemiji i hemijskoj tehnologiji, Umetnost probe, ili vodič za hemijsko ispitivanje metalnih ruda i drugih fosila (1801), Metoda za ispitivanje mineralnih voda (1800), Uputstva o najboljim načinima ekstrahovati, pripremati i prečišćavati salitru u Rusiji...” (1812). Takođe je prevodio sa francuskog i revidirao Hemijski rečnik (tom 14, 18101813), bio je osnivač i urednik (od 1804) Tehnološkog časopisa. TIH. Lovitz je otkrio (1785) fenomen adsorpcije ugljika u tečnom mediju i na osnovu toga predložio metode za pročišćavanje vode, alkohola i lijekova; dao značajan doprinos proučavanju rastvora soli i kristalohemije; razvio metode za dobijanje glacijalne sirćetne kiseline, kristalne glukoze, bezvodnog dietil etra i alkohola, kao i odvajanje soli barijuma, stroncijuma i kalcijuma. Do kraja XVIII vijeka. pojavili su se prvi radovi u Rusiji iz oblasti hemije i tehnologije platine i hroma. Počasni član Sankt Peterburgske akademije nauka A.A. Musin-Pushkin je primio niz "trostrukih" kompleksnih soli platine - magnezijum, barijum i natrijum hloroplatinate, amalgam platine, razvio je metodu za dobijanje kovljive platine kalcinacijom njenog amalgama. Bio je prvi koji je dobio i opisao sol metalne žive, otkrio krom alum i proučavao legure platine sa bakrom i srebrom.
Ako se 18. vek može nazvati periodom rađanja ruske hemijske nauke, onda 19. vek. podijeljeno je na dva perioda: prva polovina - formiranje domaće hemije, druga polovina - etabliranje ruskih naučnika u profesionalnoj svjetskoj zajednici. Istovremeno, izvanredna otkrića D.I. Mendeljejev i A.M. Butlerov je postao logična posledica ogromne aktivnosti ruskih naučnika na popularizaciji hemijskih i hemijsko-tehnoloških znanja, na razvoju domaće industrije, koju su sprovodili od početka veka. Petersburg akademije nauka, u kojoj je u XVIII vijeku. gotovo sva ruska hemija bila je koncentrisana, nije izgubila na značaju u sljedećem stoljeću. Godine 1803. usvojena je njena nova povelja u kojoj je definisana kao glavna naučna institucija zemlje, a njeni zadaci su bili unapređenje nauke, obrazovanja, kao i unapređenje manufaktura, zanata i fabrika. Godine 18101830. Ruski hemičari su uradili veliki posao na stvaranju obrazovno-metodičkih osnova za nastavu hemije, pisanju domaćih priručnika iz hemije. Dakle, 1808. godine A.I. Scherer (17721825), profesor Medicinsko-hirurške akademije u Sankt Peterburgu, Glavnog pedagoškog instituta i Rudarskog kadetskog korpusa, a od 1815. akademik Sankt Peterburške akademije nauka objavio je prvi ruski udžbenik "Vodič za nastavu hemije" (iz dva dela). U Upozorenju je pisao o svojoj želji prije svega da nastava hemije bude "praktična i temeljna". Godine 1813-1817 enciklopedijski vodič u pet tomova "Opšta hemija za školsku decu i studente" objavio je profesor hemije Univerziteta u Harkovu F.I. Giza (17841821). Ovo jedinstveno izdanje je po prvi put upoznalo ruskog čitaoca sa najnovijim teorijama i otkrićima u hemiji: idejama K. Bertholleta o hemijskom afinitetu, Prustovim zakonima, Rihterovim zakonima, G. Davyjevim i J. Berzeliusovim elektrohemijskim idejama itd. Prva knjiga koja sasvim u potpunosti odražava najnovija dostignuća nauke i koji je u kompaktnom i pristupačnom obliku predstavio činjenice i teorije hemije, postao je udžbenik G.I. Hess "The Foundation of Pure Chemistry" (1831), koji je do objavljivanja "Osnova hemije" D.I. Mendeljejeva (1869) su ruske obrazovne institucije usvojile kao glavni vodič za hemiju. Ime Hermana Ivanoviča Hessa (18021850) ušlo je u istoriju svjetske i domaće hemije ne samo zahvaljujući njegovom čuvenom udžbeniku. Prije svega, poznat je kao osnivač prve ruske naučne škole neorganskih hemičara, jedan od osnivača termohemije. U svojim termohemijskim studijama, G.I. Hess mnogo ranije od Kh.P. Thomsen i P.E. Berthelot je iznio (1840) stav prema kojem veličina termičkog efekta reakcije može poslužiti kao mjera kemijskog afiniteta. Otkrio je (1840) osnovni zakon termohemije zakon konstantnosti količine toplote, dokazao (1842) pravilo termoneutralnosti.
Druga polovina 19. veka predstavlja poseban period u istoriji domaće nauke, uključujući i hemiju. Epohu u istoriji svetske nauke bilo je otkriće 1869. godine Dmitrija Ivanoviča Mendeljejeva (1834-1907) Periodnog zakona hemijskih elemenata i razvoj u 1861-1870. A.M. Butlerov (18281886) teorija hemijska struktura supstance.
Odgovor na pitanje o razlici u hemijskim svojstvima organskih jedinjenja dao je A.M. Butlerov u svojoj teoriji hemijske strukture. Pokazao je da reaktivnost molekula zavisi od energija hemijskih veza između atoma, koje se menjaju kao rezultat međusobnog uticaja atoma i atomskih grupa u jednom molekularnom sistemu. Dakle, u skladu sa njegovom teorijom, suština hemijske strukture molekula leži u energetskoj neekvivalenciji različitih hemijskih veza, jednako označenih kao CH, ili u opštem slučaju AB.
Na osnovu teorije hemijske strukture, predstavnici Butlerovske škole izvršili su sintezu olefinskih i parafinskih ugljovodonika sastava C5C10, osnove hemije ugljovodonika, koja je kasnije postala osnova za razvoj petrohemije, koja je glavna dobavljač karburatora i dizel goriva i maziva za auto i avio-motorogradnju. Istraživanje A.M. Butlerov o polimerizaciji niskomolekularnih olefina i o sintezi ugljovodonika, izostrukture koje je proveo da bi eksperimentalno potvrdio svoju teoriju, formirale su naučnu osnovu za sintezu komponenti visokokvalitetnih avionskih goriva. Zbijanje olefinskih ugljovodonika prema Butlerovu postalo je važno i za sintezu aditiva koji poboljšavaju svojstva viskoznosti ulja za podmazivanje. Ništa manje značajan doprinos nauci o hemiji nafte dao je A.M. Butlerova, V.V. Markovnikov, koji je više od 20 godina svoje naučne aktivnosti posvetio proučavanju sastava kavkaskog ulja. Proučavanje ulja u periodu intenzivnog razvoja kavkaskih polja u poslednjoj četvrtini 19. veka bilo je koncentrisano uglavnom na Moskovskom univerzitetu u laboratorijama N.D. Zelinsky i V.V. Markovnikov. Posebna pažnja na V.V. Markovnikov se fokusirao na izdvajanje naftenskih ugljovodonika iz nafte višestrukom frakcijskom destilacijom i proučavanje svojstava ekstrahovanih ugljovodonika. Hemijske metode za identifikaciju naftnih ugljovodonika, koje je razvio naučnik, našle su primenu u svim laboratorijama sveta. Ove reakcije se koriste za sintezu mnogih organskih spojeva.
- Uloga hemije u savremenom svetu.
U atmosferi "kemifobije" mora se biti potpuno svjestan nemogućnosti društvenog napretka bez razvoja hemije i primjene njenih dostignuća u rješavanju problema energetike, ekologije, odbrane države, zdravstva, industrijskog razvoja i poljoprivrede.
Dovoljno je reći da 92% energije koju društvo trenutno troši, dobijamo izvodeći hemijske procese. A ako moderna energija stvara ekološke probleme, onda nije kriva hemija, već nepismeno ili beskrupulozno korištenje proizvoda njenog djelovanja (hemijski procesi, proizvodi, materijali).
Mora se imati na umu da hemija nije samo DDT, defolijanti, nitrati i dioksini. Ali i šećer i so, vazduh i validol, mleko i magnezijum, polietilen i penicilin. Sve što koristimo, nosimo, živimo, krećemo se, igramo se proizvodi kontroliranim kemijskim reakcijama.
Zanimanje hemičara je pronalazak reakcija koje pretvaraju supstance oko nas u one koje služe da zadovolje naše potrebe.
Moramo imati efikasan lijek za Parkinsonovu bolest. Hemičari sintetiziraju karbidofu, spoj koji se ne nalazi u prirodi, ali ima visoku terapeutsku aktivnost.
Milioni automobila zagađuju atmosferu. Ovaj problem je dijelom pomogao da se riješi automobilski katalizator izduvnih plinova.
Sada postoji više od 8 miliona sintetizovanih jedinjenja. Hemija igra ulogu u rješavanju problema obezbjeđivanja ljudi hranom, odjećom i stanovanjem, novim izvorima energije, u stvaranju obnovljivih zamjena za iscrpljujuće ili rijetke materijale, u jačanju zdravlja ljudi, u praćenju stanja životne sredine i njenoj zaštiti.
Budući da su svi životni procesi uzrokovani hemijom. promjene, poznavanje hemijskih reakcija daje neophodnu osnovu za sagledavanje suštine života. Dakle, hemija doprinosi rješavanju problema od univerzalnog filozofskog značaja.
Tragedija u Bhopalu (Indija) jasno pokazuje dvije strane hemije. Hiljade ljudi su otrovane otrovnim supstancama koje se koriste u proizvodnji hrane, spašavajući milione ljudi od gladi svake godine.
Spisak korištenih obrazovnih metoda materijala.
- Bill Stayman. "Kompletan vodič o štetnim, korisnim i neutralnim materijama koje se nalaze u hrani, kozmetici, lijekovima", "Eksmo - press", 2003.
- Bobyrev V.G., Kuzmin N.M. Fizičke i hemijske metode istraživanja. Volgograd: Viša škola Ministarstva unutrašnjih poslova, 1979.
- Gabrielyan O.S. hemija. 8. razred: udžbenik. M.: Drofa, 2011.
- Gabrielyan O.S., Lysova G.G. Tutorial za svršene razrede opšteg obrazovanja obrazovne institucije. Moskva, 2000.
- Glinka N.L. Opšta hemija: udžbenik za srednje škole / Ed. V.A. Rabinovich. L.: Hemija, 1983.
- Dorohova E.N., Prokhorova G.V. Analitička hemija. Fizičko-hemijske metode analize: Udžbenik. Moskva: Viša škola, 1991.
- Zaitsev A.N. O sigurnim aditivima za hranu i "zloslutnim" simbolima "E" časopis "Ekologija i život", br. 4, 1999.
- Kukushkin N.N. Hemija oko nas M.: Viša škola, 1992.
- Mashkovsky, M.D. Lijekovi: u 2 toma / M.D. Mashkovsky - 14. izd., revidirano. i dodatne - M.: Novi talas, 2004. - T. 1.
- Naučno-metodološki časopis "Hemija" u školi, "Centar Himpres" (za 2001-2003).
- Pichugina G.V. "Ponoviti hemiju sa primjerima iz svakodnevnog života" - Moskva: "Arkti", 2000.
- Tretyakov Yu.D. i dr. Hemija i modernost: Vodič za nastavnike. M.: Obrazovanje, 1985.
- Chernobelskaya G.M. „Metodika nastave hemije u srednjoj školi“, Moskva „Vladoš“, 2000.
- Yudin A.M., V.N. Suchkov. "Hemija za tebe". M.: Hemija, 2001
- Shulgin G.B. "Hemija za sve", Moskva, "Znanje", 1987.
- Enciklopedija za djecu. hemija. M.: Avanta +, 2005.
- www. eco. n.w. en/lib/data/07/3/030307. htm - dodaci ishrani.
- „Enciklopedija učenika. Tačne nauke." priredio P. Koshel. Olma-Press, 2004.
Zanimanje ___ Datum ___/___/_____ Razred ______
_________________________________________________________________________________________
Hemija je nauka o prirodi. Hemija u okolini. Kratke vijesti iz istorije razvoja hemije.
hemija – nauka o supstancama, njihovim svojstvima irotacije . Proučava sastav i strukturu supstanci, uslove i metode transformacije jednih supstanci u druge, kao i pojave koje prate te transformacije.
Predmet studija hemija su hemijski elementi, hemijske reakcije raznih jedinjenja
zakone koji upravljaju ovim transformacijama, kao i procese i pojave koje prate ove transformacije. Transformacija tvari s promjenom sastava molekula naziva sehemijske reakcije .
Mainzadataka iz hemije :
proučavanje supstanci i njihovih svojstava;
dobijanje supstanci sa prethodno poznatim svojstvima;
istraživanje i korišćenje energije hemijskih reakcija i pojava koje ih prate;
razvoj i intenziviranje hemijske industrije;
razvoj ekološki prihvatljivih tehnologija bez otpada.
Hemija je jedna od 6 nauka koje su usko povezane sa ljudskim aktivnostima (slika 1). Nastaje u antičko doba. U tom periodu primitivni ljudi su počeli da koriste njegove resurse i znanje. Stoga se hemija smatra jednom od najstarijih disciplina (sl. 2 a, b, c). Sada se znanje iz hemije veoma široko koristi u medicini, u prehrambenoj industriji, u poljoprivredi itd. Ne postoji nijedna industrija u kojoj hemija ne učestvuje ili ne doprinosi razvoju.
Hemija kao nauka podijeljen je na sljedeće dijelove: opći, neorganski, organski, fizički i analitički.
Slika 1. Odnos hemije sa drugim naukama
a
Slika 2. Hemija u antici
in
Slika 3. Hemijska bojeva glava
Ali, hemija ne pomaže uvek čoveku. Ako ne iskoristite njeno znanje ispravno, može ga nauditi, pa čak i ubiti. Na prvi pogled ova mala bomba (sl. 3) ne predstavlja posebno razornu silu. Zapravo – to je istina, snaga ove bombe leži u onome što se dešava nakon što eksplodira: bolna smrt, bolne opekotine, sakaćenje. Zato budite oprezni kada koristite znanje iz hemije, znajte da hemičar, kao i lekar, ima i neke etičke principe i obaveze naznačene u tekstu Hipokratove zakletve:
Svi naučnici su identifikovali nekoliko faza u formiranju hemije kao nauke.
І . Alhemijski period ( IV - XVI u.)
Cilj: potraga za kamenom filozofa za pretvaranje metala u zlato, sinteza eliksira mladosti.
Hemijsko znanje se razvijalo sporo.Slabo razvijena proizvodnja.
Otkrivene razne supstance
Stekao mnogo praktičnog iskustva u radu sa supstancama
ІІ . Period teorije flogistona ( XVII in. )
“... sve supstance u svom sastavu sadrže flogiston, kojisi tokom reakcija sagorevanja je istrošen"
1756 . Ruski naučnik M. Lomonosov je dokazao: tokom sagorevanja, supstance se kombinuju sa sastavnim česticama vazduha.1774 A. Lavoisierovo istraživanje je pokazalo da je kiseonik sastavni deo vazduha. Dakle, supstance tokom sagorevanja i oksidacije ulaze u složenu reakciju.
Pozitivno: 1. Dato je naučno objašnjenje procesa sagorevanja i oksidacije.
2. Teorija flogistona pokazala se pogrešnom
Stvaranje atomsko-molekularne teorije (M. Lomonosov, J. Dalton)
Pozitivno: razvoj hemijske nauke je stavljen na naučnu osnovu.
Uloga hemije u društvu
Proizvodnja:prehrambeni proizvodi.
Građevinski materijal.
Lakovi, ljepila, boje, keramika.
Sapun, SMZ.
Proizvodnja:
Masti, antibiotici, antiseptici, sulfa lijekovi
vitamini
Proizvodnja:
Lijevano željezo, čelik, crni i obojeni materijali.
Ultra čisti, super-tvrdi materijali otporni na toplotu.
Poljoprivreda
Hemija u životu društva
Kozmetika i parfimerija
Proizvodnja:
mineralna đubriva.
Sredstva za zaštitu bilja.
Aditivi za stočnu hranu.
Proizvodnja:
Supstance sa mirisom.
Boje za kosu.
Kreme za kožu.
Puder, ruž, šminka.
Aerosoli.
zaštite okoliša
Hemija i zaštita države
Hemija i zdravlje
Proizvodnja:
Kationski i anjonski izmjenjivači za prečišćavanje vode.
Supstance za neutralizaciju pesticida.
Supstance za deaktivaciju radioaktivnih izotopa.
Proizvodnja:
Eksplozivi
hemijsko oružje
Proizvodnja:
Sredstva protiv bolova, dezinficijensi, anestetici
Serumi, zamjene za krv
Proteze, umjetne kosti, zglobovi
Pročitajte priču i odgovorite na pitanje: „Zašto je hemija važna za društvo?“.
Želim da postanem hemičar! - ovako je gimnazijalac Justus Liebig (rođen 1803.) odgovorio na pitanje direktora gimnazije u Darmštatu o izboru budućeg zanimanja. To je izazvalo smeh nastavnika i školaraca prisutnih u razgovoru. Činjenica je da se početkom prošlog vijeka u Njemačkoj, ai u većini drugih zemalja, takva profesija nije shvaćala ozbiljno. Hemija se smatrala primijenjenim dijelom prirodne nauke, a iako su se razvijale teorijske ideje o supstancama, eksperimentu se najčešće nije pridavao odgovarajući značaj. Ali Liebig, dok je još bio u gimnaziji, bavio se eksperimentalnom hemijom. Strast prema hemijskim eksperimentima pomogla mu je u daljem istraživačkom radu. Već sa 21 godinom Liebig je postao profesor u Giessenu i organizovao jedinstvenu hemijsku školu koja je privukla mlade pristalice ove nauke iz različitih zemalja. Služio je kao prototip modernih specijalnih obrazovnih institucija. Inovacija nastave bila je u tome što su učenici mnogo pažnje posvetili eksperimentima. Samo zahvaljujući Liebigu, težište kursa hemije prebačeno je iz učionice u laboratoriju.
U današnje vrijeme želja da se postane hemičar nikoga ne zasmijava, naprotiv, hemijskoj industriji su stalno potrebni ljudi koji spajaju široko znanje i eksperimentalne vještine sa ljubavlju prema hemiji.
| 1. Studije hemije: a) sastav i svojstva supstanci; b) sastav i struktura supstance; c) sastav, struktura, svojstva supstanci i metode njihove transformacije. ________ 2. Koji poznati naučnikXVIIin. svojim radovima je pratio formiranje hemije kao nauke: a) G. Stahl; b) B. Grand; c) R. Boyle. ________ 3. Ko je od naučnika predložio teoriju sagorevanja kiseonika: a) M. Lomonosov; b) J. Priestley; c) A. Lavoisier. ________ 4. Šta je bio najvažniji rezultat aktivnosti alhemičara: a) potraga za kamenom filozofom; b) akumulacija praktičnog iskustva; c) otkriće novih supstanci. ________ 5. Ko je od naučnika predložio atomsko-molekularnu teoriju: a) R. Boyle; b) M. Lomonosov; c) J. Dalton. ________ 6. Ko je od poznatih naučnika napisao: “Danas ne može postojati specijalista koji bi mogao bez znanja hemije”: a) D. Mendeljejev; b) V. Vernadsky; c) M. Semenov. ________ 7. Ko je razvio atomsko-molekularnu teoriju: a) R. Boyle; b) J. Dalton; c) M. Lomonosov. ________ | 8. U kom slučaju je hemija štetna: a) ako ne poznajete svojstva supstanci i njihov uticaj na žive organizme; b) u slučaju nepravilne upotrebe supstanci i materijala; c) podliježu svim pravilima za rad tvari. ________ 9. Koja je teorija poslužila razvoju hemije uXIX vijek: a) teorija sagorevanja kiseonika; b) teorija elektrolitičke disocijacije; c) atomsko-molekularna teorija. ________ 10. Hemijski procesi koji se koriste u zanatstvu: a) karburacija; b) proizvodnja stakla; c) krojenje. ________ Tačni odgovori _____ pogrešni ______ Rezultat ______ bodova _________ /slikanje/ Oralno 1. Koje periode razvoja hemije poznajete? 2. Formulirajte definiciju hemije kao nauke. 3. Navedite grane upotrebe hemijskog znanja. 4. Koje su teorije bile osnova za razvoj klasične hemije (popis). 5. Šta je predmet hemije? 6. Kako razumete - "zadatke hemije kao nauke"? 7. Analizirati dostignuća i nedostatke alhemijskog perioda u razvoju hemije. 8. Vaše shvatanje - "formiranje hemije kao nauke." 9. Koje prirodne nauke poznaješ? 10. Kakvu ulogu hemija ima u razvoju: arheologija, kriminologija, astronomija? |
_______________________________________________________________________________________
Grosse E. Weissman H. Hemija za radoznale. Osnove hemije i zabavni eksperimenti. 2nd Russian Ed. - L.: Hemija, 1985 - Lajncig, 1974.
HEMIJA HISTORY
U članku se prati razvoj hemije od samog nastanka, od vremena kada je čovek naučio da vadi i održava vatru i njome topi metale iz ruda, zatim kroz doba antike i srednjeg veka do našeg vremena - perioda trijumf hemijske nauke i tehnologije.
POREKLO HEMIJE
Hemija antike. Hemija, nauka o sastavu supstanci i njihovim transformacijama, počinje tako što je čovek otkrio sposobnost vatre da menja prirodne materijale. Očigledno, ljudi su znali topiti bakar i bronzu, proizvode od vatrene gline i dobiti staklo još 4000. godine prije Krista. Do 7. v. BC. Egipat i Mesopotamija postali su centri proizvodnje boja; Na istom mjestu dobijano je zlato, srebro i drugi metali u čistom obliku. Od otprilike 1500. do 350. godine prije Krista destilacija se koristila za proizvodnju boja, a metali su se topili iz ruda miješanjem sa drvenim ugljem i upuhujući zrak kroz goruću smjesu. Samim postupcima transformacije prirodnih materijala dato je mistično značenje.
Grčka prirodna filozofija. Ove mitološke ideje prodrle su u Grčku preko Talesa iz Mileta (oko 625 - oko 547 pne), koji je svu raznolikost pojava i stvari podigao na jedan element - vodu. Međutim, grčke filozofe nisu zanimale metode dobijanja supstanci i njihova praktična upotreba, već uglavnom suština procesa koji se odvijaju u svijetu. Tako je drevni grčki filozof Anaksimen (585-525 pne) tvrdio da je osnovni princip univerzuma vazduh: kada se razrijedi, zrak se pretvara u vatru, a kako se zgušnjava, postaje voda, zatim zemlja i, konačno, kamen. Heraklit iz Efeza (kraj 6. - početak 5. vijeka prije nove ere) pokušao je objasniti prirodne pojave postulirajući vatru kao prvi element.
Četiri primarna elementa. Ove ideje su spojene u prirodnoj filozofiji Empedokla iz Agrigenta (490-430 pne) - tvorca teorije o četiri principa svemira. U različitim verzijama, njegova teorija je dominirala umovima ljudi više od dva milenijuma. Prema Empedoklu, svi materijalni objekti nastaju spajanjem vječnih i nepromjenjivih elemenata – vode, zraka, zemlje i vatre – pod utjecajem kosmičkih sila ljubavi (privlačnosti) i mržnje (odbojnosti). Teoriju o elementima Empedokla prihvatio je i razvio najprije Platon (427-347 pne), koji je precizirao da nematerijalne sile dobra i zla mogu te elemente pretvoriti jedan u drugi, a potom i Aristotel (384-322 pne). Prema Aristotelu, elementi-elementi nisu materijalne supstance, već nosioci određenih kvaliteta – toplote, hladnoće, suvoće i vlage. Ovo gledište je pretočeno u ideju o četiri Galenova "soka" (129-200. ne) i dominiralo je naukom do 17. veka. Drugo važno pitanje koje je zaokupljalo grčke prirodne filozofe bilo je pitanje djeljivosti materije. Osnivači koncepta, kasnije nazvanog "atomistički", bili su Leukip (oko 500-440 pne), njegov učenik Demokrit (oko 470-360 pne) i Epikur (oko 342-270 pne) ..e.). Prema njihovom učenju, postoje samo praznina i atomi - nedjeljivi materijalni elementi, vječni, neuništivi, neprobojni, različiti po obliku, položaju u praznini i veličini; sva tela su formirana iz njihovog "vihora". Atomistička teorija ostala je nepopularna dva milenijuma nakon Demokrita, ali nije potpuno nestala. Jedan od njegovih pristalica bio je starogrčki pjesnik Tit Lukrecije Kar (95-55. pne), koji je izložio stavove Demokrita i Epikura u pjesmi O prirodi stvari (De Rerum Natura).
Alhemija. Alhemija je umjetnost poboljšanja materije transformacijom metala u zlato i poboljšanje čovjeka stvaranjem eliksira života. U nastojanju da ostvare za njih najatraktivniji cilj - stvaranje neprocjenjivog bogatstva - alkemičari su riješili mnoge praktične probleme, otkrili mnoge nove procese, promatrali različite reakcije, doprinoseći formiranju nove nauke - kemije.
helenistički period. Egipat je bio kolevka alhemije. Egipćani su briljantno savladali primijenjenu hemiju, koja, međutim, nije bila izdvojena kao samostalna oblast znanja, već je bila uključena u "svetu tajnu umjetnost" svećenika. Kao posebna oblast znanja, alhemija se pojavila na prelazu iz 2. u 3. vek. AD Nakon smrti Aleksandra Velikog (323. pne.), njegovo carstvo je propalo, ali se uticaj Grka proširio na ogromne teritorije Bliskog i Srednjeg istoka. Alhemija je dostigla posebno brz procvat 100-300 godine nove ere. u Aleksandriji. Oko 300. godine nove ere Egipćanin Zosima je napisao enciklopediju - 28 knjiga koje pokrivaju sva znanja iz alhemije za prethodnih 5-6 vekova, a posebno informacije o međusobnim transformacijama (transmutacijama) supstanci.
Alhemija u arapskom svijetu. Osvojivši Egipat u 7. vijeku, Arapi su asimilirali grčko-orijentalnu kulturu, koju je vekovima očuvala aleksandrijska škola. Imitirajući drevne vladare, kalifi su počeli da pokroviteljuju nauke, a u 7.-9. pojavili su se prvi hemičari. Najtalentovaniji i najpoznatiji arapski alhemičar bio je Jabir ibn Hayyan (krajem 8. stoljeća), koji je kasnije postao poznat u Evropi pod imenom Geber. Džabir je vjerovao da su sumpor i živa dva suprotna principa iz kojih se formira sedam drugih metala; zlato se najteže formira: za to je potrebna posebna supstanca, koju su Grci nazvali xerion - "suvo", a Arapi su je promijenili u al-iksir (tako se pojavila riječ "eliksir"). Eliksir je trebao imati i druga čudesna svojstva: da liječi sve bolesti i daje besmrtnost. Drugi arapski alhemičar, ar-Razi (oko 865-925) (poznat u Evropi kao Razes) također se bavio medicinom. Dakle, opisao je način pripreme gipsa i način nanošenja zavoja na mjesto prijeloma. Međutim, najpoznatiji liječnik bio je Bukharan Ibn Sina (oko 980-1037), također poznat kao Avicena. Njegovi spisi su služili kao vodič za lekare tokom mnogih vekova.
Alhemija u zapadnoj Evropi. Naučni pogledi Arapa prodrli su u srednjovjekovnu Evropu u 12. vijeku. kroz sjevernu Afriku, Siciliju i Španiju. Djela arapskih alhemičara prevedena su na latinski, a zatim i na druge evropske jezike. U početku se alhemija u Evropi oslanjala na rad svetila kao što je Džabir, ali tri veka kasnije ponovo je došlo do ponovnog interesovanja za učenja Aristotela, posebno za spise nemačkog filozofa i dominikanskog teologa, koji je kasnije postao biskup i profesor. na Univerzitetu u Parizu, Albert Veliki (oko 1200-1280) i njegov učenik Toma Akvinski. Uvjeren u kompatibilnost grčke i arapske nauke s kršćanskom doktrinom, Albertus Magnus je potaknuo njihovo uvođenje u školske programe. Godine 1250. Aristotelova filozofija je uvedena u nastavni plan i program na Univerzitetu u Parizu. Engleski filozof i prirodnjak, franjevački redovnik Roger Bacon (1214-1294), koji je anticipirao mnoga kasnija otkrića, također je bio zainteresiran za alhemijske probleme; proučavao je svojstva salitre i mnogih drugih supstanci, pronašao način da napravi crni prah. Ostali evropski alhemičari su Arnaldo da Villanova (1235-1313), Raymond Lull (1235-1313), Basil Valentin (njemački monah iz 15.-16. stoljeća).
Dostignuća alhemije. Razvoj zanatstva i trgovine, uspon gradova u zapadnoj Evropi u 12.-13. veku. praćen razvojem nauke i nastankom industrije. Recepti alhemičara korišteni su u tehnološkim procesima kao što je obrada metala. Tokom ovih godina počela su sistematska potraga za metodama za dobijanje i identifikaciju novih supstanci. Postoje recepti za proizvodnju alkohola i poboljšanja u procesu njegove destilacije. Najvažnije dostignuće bilo je otkriće jakih kiselina - sumporne, azotne. Sada su evropski hemičari mogli da izvedu mnoge nove reakcije i dobiju supstance kao što su soli azotne kiseline, vitriola, stipse, soli sumporne i hlorovodonične kiseline. Usluge alhemičara, koji su često bili vješti ljekari, koristilo je najviše plemstvo. Također se vjerovalo da alhemičari posjeduju tajnu pretvaranja običnih metala u zlato.

U "LABORATORIJI" ALHEMIČARA
Do kraja 14. vijeka Interes alhemičara za pretvaranje jednih supstanci u druge ustupio je mjesto interesu za proizvodnju bakra, mesinga, octa, maslinovog ulja i raznih lijekova. U 15-16 veku. iskustvo alhemičara sve se više koristilo u rudarstvu i medicini.
POREKLO SAVREMENE HEMIJE
Kraj srednjeg vijeka obilježen je postepenim odmakom od okultizma, opadanjem interesovanja za alhemiju i širenjem mehaničkog pogleda na strukturu prirode.
Iatrochemistry. Sasvim drugačije poglede na ciljeve alhemije imao je Paracelzus (1493-1541). Pod takvim imenom koje je on odabrao ("superior Celsus"), švajcarski doktor Philipp von Hohenheim ušao je u istoriju. Paracelsus je, poput Avicene, vjerovao da glavni zadatak alhemije nije traženje načina za dobivanje zlata, već proizvodnja lijekova. On je iz alhemijske tradicije pozajmio doktrinu da postoje tri glavna dela materije - živa, sumpor, so, koji odgovaraju svojstvima isparljivosti, zapaljivosti i tvrdoće. Ova tri elementa čine osnovu makrokosmosa (Univerzuma) i povezana su sa mikrokosmosom (čovekom) formiranim od duha, duše i tela. Okrećući se definiciji uzroka bolesti, Paracelzus je tvrdio da groznica i kuga dolaze od viška sumpora u tijelu, paraliza se javlja s viškom žive itd. Princip kojeg su se svi jatrohemičari pridržavali je da je medicina stvar hemije, a sve zavisi od sposobnosti doktora da izoluje čiste principe od nečistih supstanci. Prema ovoj shemi, sve funkcije tijela bile su svedene na hemijske procese, a zadatak alhemičara je bio da pronađe i pripremi hemikalije za medicinske svrhe. Glavni predstavnici jatrohemijskog pravca bili su Jan Helmont (1577-1644), doktor po profesiji; Francis Silvius (1614-1672), koji je uživao veliku slavu kao ljekar i eliminirao "duhovne" principe iz jatrohemijske doktrine; Andreas Libavius (oko 1550-1616), ljekar iz Rothenburga Njihova istraživanja su u velikoj mjeri doprinijela formiranju hemije kao samostalne nauke.
mehanička filozofija. Sa sve manjim uticajem jatrohemije, prirodni filozofi su se ponovo okrenuli učenju starih o prirodi. Prvi plan u 17. veku. izašli su atomistički (korpuskularni) pogledi. Jedan od najistaknutijih naučnika - autora korpuskularne teorije - bio je filozof i matematičar Rene Descartes (1596-1650). Svoje je stavove iznio 1637. godine u svom Diskursu o metodi. Descartes je vjerovao da se sva tijela "sastoje od brojnih malih čestica različitih oblika i veličina, ... koje nisu toliko blizu jedna drugoj da oko njih nema praznina; te praznine nisu prazne, već ispunjene ... razrijeđenim stvar." Descartes svoje "male čestice" nije smatrao atomima; nedjeljiv; stajao je na stanovištu beskonačne deljivosti materije i poricao postojanje praznine. Jedan od najistaknutijih Descartesovih protivnika bio je francuski fizičar i filozof Pjer Gasendi (1592-1655). Atomizam Gasendi je u suštini bio prepričavanje Epikurovog učenja, međutim, za razliku od potonjeg, Gasendi je priznao stvaranje atoma od strane Boga; vjerovao je da je Bog stvorio određeni broj nedjeljivih i neprobojnih atoma, od kojih su sva tijela sastavljena; mora postojati apsolutna praznina između atoma. U razvoju hemije u 17. veku. posebna uloga pripada irskom naučniku Robertu Bojlu (1627-1691). Boyle nije prihvatio izjave antičkih filozofa, koji su vjerovali da se elementi svemira mogu utvrditi spekulativno; to se odražava u naslovu njegove knjige Skeptični hemičar. Kao pobornik eksperimentalnog pristupa definiciji hemijskih elemenata (koji je na kraju i usvojen), nije znao za postojanje stvarnih elemenata, iako je jedan od njih - fosfor - skoro sam otkrio. Boyleu se obično pripisuje uvođenje pojma "analiza" u hemiju. U svojim eksperimentima na kvalitativnoj analizi koristio je različite indikatore, uveo koncept hemijskog afiniteta. Na osnovu radova Galilea Galileia (1564-1642) i Evangeliste Torricellija (1608-1647), kao i Otta Guerickea (1602-1686), koji je 1654. demonstrirao "magdeburške hemisfere", Boyle je opisao vazdušnu pumpu koju je dizajnirao i eksperimentisao za određivanje elastičnosti zraka korištenjem U-cijevi. Kao rezultat ovih eksperimenata, formulisan je dobro poznati zakon o obrnutoj proporcionalnosti zapremine i pritiska vazduha. Godine 1668. Boyle je postao aktivan član novoorganizovanog Kraljevskog društva u Londonu, a 1680. je izabran za njegovog predsjednika.
Tehnička hemija. Naučni napredak i otkrića nisu mogli a da ne utiču na tehničku hemiju, čiji se elementi mogu naći u 15.-17. veku. Sredinom 15. vijeka razvijena je tehnologija puhala. Potrebe vojne industrije potaknule su rad na poboljšanju tehnologije proizvodnje baruta. Tokom 16. veka proizvodnja zlata se udvostručila, a proizvodnja srebra devet puta. Postoje temeljni radovi na proizvodnji metala i raznih materijala koji se koriste u građevinarstvu, u proizvodnji stakla, bojenju tkanina, za konzerviranje prehrambenih proizvoda i obradi kože. Sa širenjem potrošnje alkoholnih pića, unapređuju se metode destilacije, konstruišu se novi aparati za destilaciju. Pojavljuju se brojne proizvodne laboratorije, prvenstveno metalurške. Među hemijskim tehnolozima tog vremena može se spomenuti Vannoccio Biringuccio (1480-1539), čije je klasično djelo O pirotehnici objavljeno u Veneciji 1540. godine i sadržavalo je 10 knjiga, koje su se bavile rudnicima, ispitivanjem minerala, pripremanjem metala, destilacijom, vojnom umjetnošću. i vatromet. Još jednu čuvenu raspravu, O rudarstvu i metalurgiji, napisao je George Agricola (1494-1555). Treba spomenuti i Johanna Glaubera (1604-1670), holandskog hemičara, tvorca Glauberove soli.
XVIII VEK
Hemija kao naučna disciplina. Od 1670. do 1800. hemija je uz prirodnu filozofiju i medicinu dobila službeni status u nastavnim planovima i programima vodećih univerziteta. Godine 1675. pojavio se udžbenik Nicolasa Lemeryja (1645-1715) Kurs hemije, koji je stekao ogromnu popularnost, objavljeno je 13 njegovih francuskih izdanja, a osim toga preveden je na latinski i mnoge druge evropske jezike. U 18. vijeku u Evropi se stvaraju naučna hemijska društva i veliki broj naučni instituti; njihova istraživanja su usko povezana sa društvenim i ekonomskim potrebama društva. Pojavljuju se praktičari hemičari koji se bave proizvodnjom uređaja i pripremom supstanci za industriju.
Teorija flogistona. U spisima hemičara iz druge polovine 17. veka. mnogo pažnje je posvećeno tumačenju procesa sagorevanja. Prema idejama starih Grka, sve što može da gori sadrži element vatre, koji se oslobađa pod odgovarajućim uslovima. Godine 1669. njemački hemičar Johann Joachim Becher (1635-1682) pokušao je da racionalizira zapaljivost. Predložio je da se čvrsta tijela sastoje od tri vrste "zemlje", a jednu od vrsta, koju je nazvao "masna zemlja", uzeo je za "princip zapaljivosti". Becherov sljedbenik, njemački hemičar i liječnik Georg Ernst Stahl (1659-1734) transformirao je koncept "debele zemlje" u generaliziranu doktrinu flogistona - "početka zapaljivosti". Prema Stahlu, flogiston je određena tvar sadržana u svim zapaljivim tvarima i koja se oslobađa tijekom sagorijevanja. Stahl je tvrdio da je rđanje metala slično sagorijevanju drveta. Metali sadrže flogiston, ali rđa (šljunak) više ne sadrži flogiston. To je dalo prihvatljivo objašnjenje za proces pretvaranja ruda u metale: ruda, u kojoj je sadržaj flogistona zanemarljiv, zagrijava se na drvenom uglju bogatom flogistonom, a ovaj se pretvara u rudu. Ugalj se pretvara u pepeo, a ruda u metal bogat flogistonom. Do 1780. godine hemičari su teoriju flogistona gotovo univerzalno prihvatili, iako nije dala odgovor na vrlo važno pitanje: zašto željezo postaje teže kada zarđa, iako flogiston iz njega izlazi? Hemičari 18. veka. ova kontradikcija nije izgledala toliko važna; glavna stvar, po njihovom mišljenju, bilo je objasniti razloge za promjenu izgleda tvari. U 18. vijeku radili su mnogi hemičari čija se naučna aktivnost ne uklapa u uobičajene sheme za razmatranje faza i pravaca razvoja nauke, a među njima posebno mjesto pripada ruskom naučniku-enciklopedisti, pjesniku, prvaku obrazovanja Mihailu Vasiljeviču Lomonosovu (1711. -1765). Lomonosov je svojim otkrićima obogatio gotovo sve oblasti znanja, a mnoge njegove ideje bile su više od sto godina ispred nauke tog vremena. Godine 1756. Lomonosov je izveo čuvene eksperimente pečenja metala u zatvorenoj posudi, koji su dali neosporne dokaze o očuvanju materije u hemijskim reakcijama i ulozi vazduha u procesima sagorevanja: još pre Lavoazijea, objasnio je uočeno povećanje težine tokom pečenja. metala kombinovanjem sa vazduhom. Za razliku od preovlađujućih ideja o kalorijama, on je tvrdio da su toplinski fenomeni posljedica mehaničkog kretanja materijalnih čestica. On je objasnio elastičnost gasova kretanjem čestica. Lomonosov je pravio razliku između pojmova "telešca" (molekula) i "elementa" (atoma), što je opštepriznato tek sredinom 19. veka. Lomonosov je formulisao princip očuvanja materije i kretanja, isključio flogiston iz broja hemijskih agenasa, postavio temelje fizičke hemije, a 1748. godine stvorio hemijsku laboratoriju pri Sankt Peterburškoj akademiji nauka, u kojoj ne rade samo naučni radovi. održana je, ali i praktična nastava za studente. Sproveo je opsežna istraživanja u oblastima znanja koje su bliske hemiji - fizici, geologiji, itd.
Pneumatska hemija. Nedostaci teorije flogistona najjasnije su se otkrili tokom razvoja tzv. pneumatska hemija. Najveći predstavnik ovog pravca bio je R. Boyle: on ne samo da je otkrio zakon o plinu, koji sada nosi njegovo ime, već je dizajnirao i aparat za sakupljanje zraka. Hemičari su dobili najvažnije oruđe za izolaciju, identifikaciju i proučavanje raznih "vazduha". Važan korak bio je izum engleskog hemičara Stephena Halesa (1677-1761) "pneumatske kupke" početkom 18. vijeka. - uređaj za hvatanje gasova koji se oslobađaju prilikom zagrevanja supstance u posudu sa vodom, spuštenu naopačke u kadu sa vodom. Kasnije su Hales i Henry Cavendish (1731-1810) ustanovili postojanje određenih plinova ("vazduha") koji se po svojim svojstvima razlikuju od običnog zraka. Godine 1766, Cavendish je sistematski proučavao gas koji nastaje tokom interakcije kiselina sa određenim metalima, kasnije nazvan vodonikom. Veliki doprinos proučavanju gasova dao je škotski hemičar Joseph Black (1728-1799). Počeo je proučavati plinove koji se oslobađaju djelovanjem kiselina na alkalije. Black je otkrio da se mineral kalcijev karbonat, kada se zagrije, razgrađuje s oslobađanjem plina i formira vapno (kalcij oksid). Oslobođeni plin (ugljični dioksid - Black ga je nazvao "vezani zrak") mogao bi se rekombinovati sa vapnom da bi se formirao kalcijum karbonat. Između ostalog, ovim otkrićem je utvrđena neraskidivost veza između čvrstih i plinovitih tvari.
hemijska revolucija. Joseph Priestley (1733-1804), protestantski svećenik koji je bio strastven za hemiju, postigao je veliki uspjeh u izolaciji plinova i proučavanju njihovih svojstava. U blizini Leedsa (Engleska), gdje je služio, postojala je pivara, odakle je bilo moguće dobiti "vezani zrak" (sada znamo da je to bio ugljični dioksid) u velikim količinama za eksperimente. Priestley je otkrio da se plinovi mogu otopiti u vodi i pokušao ih prikupiti ne preko vode, već preko žive. Tako je uspio prikupiti i proučavati dušikov oksid, amonijak, klorovodik, sumpor-dioksid (naravno, ovo su njihova moderna imena). Godine 1774. Priestley je napravio svoje najvažnije otkriće: izolirao je plin u kojem su tvari posebno žarko gorjele. Kao pristalica teorije flogistona, on je ovaj plin nazvao "deflogisticiranim zrakom". Činilo se da je plin koji je Priestley otkrio suprotan "flogisticiranom zraku" (azotu) koji je 1772. izolirao engleski hemičar Daniel Rutherford (1749-1819). U "flogisticiranom zraku" miševi su uginuli, dok su u "deflogisticiranom" bili vrlo aktivni. (Treba napomenuti da je svojstva gasa koji je izolovao Priestley opisao švedski hemičar Carl Wilhelm Scheele (1742-1786) još 1771. godine, ali se njegova poruka, zbog nemara izdavača, pojavila u štampi tek godine. 1777.) Veliki francuski hemičar Antoine Laurent Lavoisier (1743-1794) odmah je shvatio značaj Priestlijevog otkrića. Godine 1775. pripremio je članak u kojem je tvrdio da zrak nije jednostavna supstanca, već mješavina dva plina, jedan od njih je Priestleyjev "deflogisticirani zrak", koji se kombinira sa zapaljenim ili zarđalim predmetima, prelazi iz rude u drveni ugalj i neophodno za život. Lavoisier ga je nazvao kiseonikom, kiseonikom, tj. "proizvođač kiselina". Drugi udarac teoriji elementarnih elemenata zadat je nakon što je postalo jasno da voda također nije jednostavna supstanca, već proizvod kombinacije dvaju plinova: kisika i vodika. Sva ova otkrića i teorije, ukinuvši misteriozne "elemente", dovela su do racionalizacije hemije. Došle su do izražaja samo one supstance koje se mogu izvagati ili čija se količina može na neki drugi način izmjeriti. Tokom 80-ih godina 18. vijeka. Lavoisier, u saradnji sa drugim francuskim hemičarima - Antoine Francois de Fourcroix (1755-1809), Guiton de Morveau (1737-1816) i Claude Louis Berthollet (1748-1822) - razvio je logički sistem hemijske nomenklature; u njemu je opisano više od 30 jednostavnih supstanci, što ukazuje na njihova svojstva. Ovo delo, Metoda hemijske nomenklature, objavljeno je 1787. Revolucija u teorijskim pogledima hemičara, koja se dogodila krajem 18. veka. kao rezultat brzog nakupljanja eksperimentalnog materijala pod dominacijom teorije flogistona (iako neovisno o njoj), obično se naziva "kemijska revolucija".
DEVETNAESTO STOLJECE
Sastav supstanci i njihova klasifikacija. Lavoisierovi uspjesi pokazali su da upotreba kvantitativnih metoda može pomoći u određivanju hemijskog sastava supstanci i razjašnjavanju zakona njihovog povezivanja.
Atomska teorija. Engleski hemičar Džon Dalton (1766-1844), kao i antički atomisti, polazio je od koncepta korpuskularne strukture materije, ali je, na osnovu koncepta Lavoazierovih hemijskih elemenata, prihvatio da "atomi" (ovaj termin Dalton je zadržao kao danak Demokritu) datog elementa su identični i karakteriše ih, između ostalih svojstava, i činjenica da imaju određenu težinu, koju je nazvao atomskom. Dalton je otkrio da se dva elementa mogu kombinirati jedan s drugim u različitim omjerima, a svaka nova kombinacija elemenata daje novu vezu. Godine 1803. ovi rezultati su generalizirani u obliku zakona višestrukih omjera. Godine 1808. objavljen je Daltonov rad, Novi sistem kemijske filozofije, u kojem je detaljno iznio svoju atomsku teoriju. Iste godine, francuski hemičar Joseph Louis Gay-Lussac (1778-1850) objavio je pretpostavku da su zapremine gasova koji reaguju jedni na druge povezane jedni s drugima kao jednostavni umnošci (zakon zapreminskih odnosa). Nažalost, Dalton nije uspio vidjeti u zaključcima Gay-Lussaca ništa osim prepreke razvoju njegove teorije, iako bi ovi zaključci mogli biti vrlo plodonosni u određivanju relativnih atomskih težina.
hemijski afinitet. Tokom celog 17. veka hemičari, govoreći o "afinitetu" - sklonosti atoma da formiraju jedinjenja - slijedili su ideje Bechera i Stahla, koji su sve supstance klasifikovali prema njihovoj sposobnosti da reaguju sa specifičnim kiselinama. Proučavanje afiniteta i sastava raznih vrsta supstanci je početkom 19. stoljeća krenulo drugačijim tokom. otkrićem nove analitičke metode. Godine 1807., engleski hemičar Humphry Davy (1778-1829) propušta električnu struju iz baterije od 250 metalnih ploča kroz rastopljeni potaš (kalijev karbonat) i dobija male kuglice metala, kasnije nazvane kalijum, a zatim izoluje natrijum iz sode u isti put. Davy je sugerirao da se kemijski afinitet svodi na elektrifikaciju atoma nakon kontakta. Švedski hemičar Jens Jakob Berzelius (1779-1848) je rafinirao i razvio ideju atoma i električnog afiniteta, predlažući prvi koncept hemijska interakcija- elektrohemijska teorija. Berzelius je vjerovao da, budući da se soli u otopini pod djelovanjem električne struje razlažu na negativne i pozitivne komponente, sva jedinjenja moraju biti sastavljena od pozitivnih i negativnih dijelova - radikala (dualistička teorija Berzeliusa). Kiseonik je najelektronegativniji element, a oni elementi koji sa njim formiraju spojeve sa svojstvima baza su elektropozitivni, a oni koji formiraju supstance sa kiselim svojstvima su elektronegativni. U skladu s tim, Berzelius je dobio ljestvicu elemenata, čiji je prvi član bio kisik, a zatim sumpor, dušik, fosfor itd. sa prelaskom preko vodonika u natrijum, kalij i druge metale. Do 1840-ih, međutim, postalo je jasno da elektrohemijska teorija ne može objasniti postojanje jednostavnih dvoatomskih molekula (kao što su O2 i H2) ili zamjenu vodonika (pozitivan afinitet) hlorom (negativni afinitet).
Klasifikacija prema atomskoj težini. Od Daltonovog vremena do 1860. u hemiji nije postojala precizna definicija atomske težine. Sistem "ekvivalentnih težina" koji je predložio engleski hemičar William Wollaston (1766-1828) oslanjao se na omjere u kojima se elementi mogu kombinovati i svaki hemičar je mogao napraviti svoju listu atomskih težina. Nije bilo polazne tačke za stvaranje sistema elemenata i dogovora o tome kako izraziti sastav jedinjenja. Godine 1860, na prvom međunarodnom hemijskom kongresu u Karlsruheu (Nemačka), italijanski hemičar Stanislao Cannizzaro (1826-1910) ponovo je oživeo zaboravljenu hipotezu svog sunarodnika Amedea Avogadra (1776-1856), koji je na osnovu otkrića zakon zapreminskih odnosa po Gay-Lussac-u, sugerisao je da jednake zapremine gasova sadrže isti broj molekula. Cannizzaro je tvrdio da se uz pomoć Avogadrove hipoteze može razlikovati koncepte "atomske težine" i "molekularne težine" za plinovite elemente i razjasniti pitanje atomske težine općenito. Godine 1869., veliki ruski hemičar Dmitrij Ivanovič Mendeljejev, koji je bio prisutan na kongresu u Karlsruheu i čuo Cannizzarov izveštaj, objavio je svoj periodni sistem. On je sve poznate elemente rasporedio u skladu s povećanjem njihove atomske težine i podijelio ih u periode i grupe koje odgovaraju promjeni valencije. U tabeli su ostavljena prazna mjesta za stavke koje još nisu otkrivene; Mendeljejev je nekima od njih čak dodijelio imena (ekabor, ekaaluminij i ekasilicij; prefiks "eka" znači "jedno te isto"). Izuzetnu tačnost periodičnog zakona pokazala su otkrića galija 1875. godine, identičnog svojstvima ekaaluminijumu, skandijumu (ekabor) 1879. i germanijumu (eka-silicijumu) 1886. godine.
Organska hemija. Tokom celog 18. veka po pitanju hemijskih odnosa između organizama i supstanci, naučnici su se rukovodili doktrinom vitalizma - doktrinom koja je život smatrala posebnim fenomenom, koji nije podložan zakonima univerzuma, već uticajem posebnih vitalnost. Ovo gledište su naslijedili mnogi naučnici 19. stoljeća, iako su njegovi temelji poljuljani još 1777. godine, kada je Lavoisier sugerirao da je disanje proces analogan sagorijevanju. Prvi eksperimentalni dokazi o jedinstvu neorganskog i organskog svijeta dobiveni su početkom 19. stoljeća. Godine 1828. njemački hemičar Friedrich Wöhler (1800-1882), zagrijavajući amonijum cijanat (ovo jedinjenje se bezuslovno smatralo neorganskom supstancom), dobio je ureu, otpadni proizvod ljudi i životinja. Godine 1845. Adolf Kolbe (1818-1884), Wöhlerov učenik, sintetizirao je sirćetnu kiselinu iz polaznih elemenata ugljenika, vodonika i kiseonika. 1850-ih, francuski hemičar Pierre Berthelot (1827-1907) započeo je sistematski rad na sintezi organskih jedinjenja i dobio metil i etil alkohole, metan, benzol i acetilen. Sistematsko proučavanje prirodnih organskih spojeva pokazalo je da svi sadrže jedan ili više atoma ugljika i vrlo mnogo atoma vodika. Kao rezultat svih ovih studija, njemački hemičar Friedrich August Kekule (1829-1896) je 1867. godine definirao organsku hemiju kao hemiju ugljikovih spojeva. Novi pristup organskoj analizi sažeo je njemački hemičar Justus Liebig (1803-1873) - tvorac čuvene istraživačke i nastavne laboratorije na Univerzitetu Giessen. Godine 1837. Liebig je zajedno s francuskim hemičarem Jean Baptisteom Dumasom (1800-1884) precizirao koncept radikala kao specifične, nepromijenjene grupe atoma koja je dio mnogih organskih spojeva (primjer je metil radikal CH3). Postalo je jasno da se struktura velikih molekula može odrediti samo uspostavljanjem strukture određenog broja radikala.
Teorija tipova. Otkriće i izolacija ogromnog broja složenih spojeva koji sadrže ugljik oštro je postavilo pitanje sastava njihovih molekula i dovelo do potrebe za revizijom postojeći sistem klasifikacija. Do 1840-ih, hemičari su shvatili da se Berzeliusove dualističke ideje odnose samo na neorganske soli. Godine 1853. pokušano je klasifikovati sva organska jedinjenja po vrsti. Generaliziranu "teoriju tipova" predložio je francuski hemičar Charles Frédéric Gérard (1816-1856), koji je vjerovao da kombinacija različitih grupa atoma nije određena električnim nabojem ovih grupa, već njihovim specifičnim kemijskim svojstvima. Gerard je identificirao četiri glavne vrste atomskih grupa, od kojih su, po njegovom mišljenju, sastavljena sva jedinjenja, i organska i neorganska.
Strukturna hemija. Godine 1857. Kekule je, polazeći od teorije valencije (pod valentnošću se podrazumijevao broj atoma vodika koji se spajaju s jednim atomom datog elementa), sugerirao da je ugljik četverovalentan i da se stoga može kombinirati s četiri druga atoma, formirajući dugačke lance. - ravni ili razgranati. Stoga su se organske molekule počele prikazivati ne kao kombinacije radikala, već kao strukturne formule - atomi i veze između njih. Do 1860-ih, rad Kekulea i ruskog hemičara Aleksandra Mihajloviča Butlerova (1828-1886) postavio je temelje strukturnoj hemiji, koja omogućava objašnjenje svojstava supstanci na osnovu rasporeda atoma u njihovim molekulima. 1874. danski hemičar Jacob van't Hoff (1852-1911) i francuski hemičar Joseph Achille Le Bel (1847-1930) proširili su ovu ideju na raspored atoma u svemiru. Vjerovali su da molekuli nisu ravne, već trodimenzionalne strukture. Ovaj koncept je omogućio da se objasne mnoge dobro poznate pojave, na primjer, prostorna izomerija, postojanje molekula istog sastava, ali sa različita svojstva. U to se vrlo dobro uklapaju podaci Louisa Pasteura (1822-1895) o izomerima vinske kiseline. Do kraja 19. vijeka ideje strukturne hemije potkrepljene su podacima dobijenim spektroskopskim metodama. Ove metode su omogućile dobijanje informacija o strukturi molekula na osnovu njihovih apsorpcionih spektra. Do 1900. godine koncept trodimenzionalne organizacije molekula - i složenih organskih i neorganskih - prihvaćen je od strane gotovo svih naučnika.
Chemical Technology. Napredak u organskoj hemiji podstakao je brz razvoj hemijske industrije, prvenstveno u Nemačkoj. Razvijena je tehnologija za proizvodnju sumporne kiseline, na osnovu koje se dobijaju eksplozivi, boje i soda, neophodni za proizvodnju izbjeljivača i sapuna. Veoma važnu ulogu u razvoju hemijske tehnologije odigrao je rad Liebiga i čitave plejade njegovih učenika. Kao rezultat njihovih aktivnosti, hemijska đubriva su počela da se koriste u poljoprivredi i osnovana su preduzeća za njihovu proizvodnju. Brzi razvoj njemačke industrije boja povezan je s radom Adolfa von Bayera (1835-1917) na indigu i drugim bojama, a industrijska sinteza amonijaka pod visokim pritiskom sa radom Fritza Habera (1868-1934).
Rođenje fizičke hemije. Do kraja 19. vijeka pojavili su se prvi radovi u kojima su sistematski proučavana fizička svojstva različitih supstanci (tačke ključanja i topljenja, rastvorljivost, molekulska težina). Takve studije su pokrenuli Gay-Lussac i van't Hoff, koji su pokazali da rastvorljivost soli zavisi od temperature i pritiska. Godine 1867. norveški hemičari Peter Waage (1833-1900) i Kato Maximilian Guldberg (1836-1902) formulirali su zakon djelovanja mase, prema kojem brzina reakcije ovisi o koncentraciji reaktanata. Matematički aparat koji su koristili omogućio je pronalaženje veoma važne veličine koja karakteriše bilo koju hemijsku reakciju – konstantu brzine.
Hemijska termodinamika. U međuvremenu, hemičari su se okrenuli centralnom pitanju fizičke hemije – uticaju toplote na hemijske reakcije. Do sredine 19. vijeka. fizičari William Thomson (Lord Kelvin) (1824-1907), Ludwig Boltzmann (1844-1906) i James Maxwell (1831-1879) razvili su nove poglede na prirodu topline. Odbacujući Lavoisierovu kaloričnu teoriju, predstavili su toplotu kao rezultat kretanja. Njihove ideje razvio je Rudolf Clausius (1822-1888). Razvio je kinetičku teoriju, prema kojoj se veličine poput volumena, tlaka, temperature, viskoznosti i brzine reakcije mogu razmatrati na temelju ideje kontinuiranog kretanja molekula i njihovih sudara. Istovremeno sa Thomsonom (1850), Clasius je dao prvu formulaciju drugog zakona termodinamike, uveo koncepte entropije (1865), idealnog gasa i slobodnog puta molekula. Termodinamički pristup hemijskim reakcijama je u svojim radovima primenio August Friedrich Gorstmann (1842-1929), koji je, na osnovu Clausiusovih ideja, pokušao da objasni disocijaciju soli u rastvoru. Godine 1874-1878 američki hemičar Josiah Willard Gibbs (1839-1903) preduzeo je sistematsko proučavanje termodinamika hemijskih reakcija. Uveo je pojam slobodne energije i hemijskog potencijala, objasnio suštinu zakona delovanja mase, primenio termodinamičke principe u proučavanju ravnoteže između različitih faza pri različitim temperaturama, pritiscima i koncentracijama (fazno pravilo). Gibbsov rad je postavio temelje moderne hemijske termodinamike. Švedski hemičar Svante August Arrhenius (1859-1927) stvorio je teoriju ionske disocijacije, koja objašnjava mnoge elektrohemijske pojave, i uveo koncept energije aktivacije. Također je razvio elektrohemijsku metodu za mjerenje molekulske težine otopljenih tvari. Istaknuti naučnik, zahvaljujući kome je fizička hemija prepoznata kao samostalna oblast znanja, bio je nemački hemičar Wilhelm Ostwald (1853-1932), koji je primenio Gibsove koncepte u proučavanju katalize. Godine 1886. napisao je prvi udžbenik fizičke hemije, a 1887. je osnovao (zajedno sa van't Hoffom) časopis Fizička hemija (Zeitschrift fr physikalische Chemie).
Dvadeseti vek
Nova konstrukcijska teorija. Sa razvojem fizičkih teorija o strukturi atoma i molekula, stari koncepti kao što su hemijski afinitet i transmutacija su ponovo promišljani. Pojavile su se nove ideje o strukturi materije.
Model atoma. Godine 1896. Antoine Henri Becquerel (1852-1908) otkrio je fenomen radioaktivnosti, otkrivši spontanu emisiju subatomskih čestica soli uranijuma, a dvije godine kasnije supružnici Pierre Curie (1859-1906) i Marie Sklodowska1867 1934) izolovao dva radioaktivna elementa: polonijum i radijum. U narednim godinama otkriveno je da radioaktivne tvari emituju tri vrste zračenja: a-čestice, b-čestice i g-zrake. Zajedno sa otkrićem Fredericka Soddyja (1877-1956), koje je pokazalo da se tokom radioaktivnog raspadanja neke supstance pretvaraju u druge, sve je to dalo novo značenje onome što su stari ljudi nazivali transmutacijom. Godine 1897. Joseph John Thomson (1856-1940) otkrio je elektron, čiji je naboj 1909. s velikom preciznošću izmjerio Robert Milliken (1868-1953). Godine 1911. Ernst Rutherford (1871-1937), zasnovan na Tomsonovom elektronskom konceptu, predložio je model atoma: pozitivno nabijeno jezgro je u središtu atoma, a negativno nabijeni elektroni kruže oko njega. Godine 1913. Niels Bohr (1885-1962), koristeći principe kvantne mehanike, pokazao je da se elektroni mogu locirati ne u bilo kojoj, već u strogo definiranim orbitama. Rutherford-Bohr planetarni kvantni model atoma primorao je naučnike da zauzmu novi pristup objašnjavanju strukture i svojstava hemijskih jedinjenja. Njemački fizičar Walter Kossel (1888-1956) sugerirao je da su hemijska svojstva atoma određena brojem elektrona u njegovoj vanjskoj ljusci, a formiranje kemijskih veza uglavnom je određeno silama elektrostatičke interakcije. Američki naučnici Gilbert Newton Lewis (1875-1946) i Irving Langmuir (1881-1957) formulisali su elektronsku teoriju hemijskog vezivanja. U skladu sa ovim idejama, molekuli anorganskih soli se stabilizuju elektrostatičkim interakcijama između njihovih sastavnih jona, koji nastaju prilikom prelaska elektrona sa jednog elementa na drugi (jonska veza), a molekuli organskih jedinjenja se stabilizuju usled socijalizacija elektrona (kovalentna veza). Ove ideje su u osnovi modernih ideja o hemijskoj vezi.
Nove metode istraživanja. Sve nove ideje o strukturi materije mogle su se formirati samo kao rezultat razvoja u 20. veku. eksperimentalna tehnika i pojava novih istraživačkih metoda. Otkriće rendgenskih zraka 1895. od strane Wilhelma Conrada Roentgena (1845-1923) poslužilo je kao osnova za kasnije stvaranje metode rendgenske kristalografije, koja omogućava određivanje strukture molekula iz uzorka rendgenske difrakcije. na kristalima. Uz pomoć ove metode dešifrovana je struktura složenih organskih jedinjenja - insulina, deoksiribonukleinske kiseline (DNK), hemoglobina itd. Stvaranjem atomske teorije pojavile su se nove moćne spektroskopske metode koje daju informacije o strukturi atoma. i molekule. Različiti biološki procesi, kao i mehanizam hemijskih reakcija, proučavaju se korišćenjem radioizotopskih oznaka; Metode zračenja također se široko koriste u medicini.
Biohemija. Ova naučna disciplina, koja se bavi proučavanjem hemijskih svojstava bioloških supstanci, u početku je bila jedna od grana organske hemije. Kao samostalna regija nastala je u poslednjoj deceniji 19. veka. kao rezultat istraživanja hemijskih svojstava supstanci biljnog i životinjskog porekla. Jedan od prvih biohemičara bio je njemački naučnik Emil Fischer (1852-1919). Sintetizovao je supstance kao što su kofein, fenobarbital, glukoza, mnoge ugljovodonike, dao veliki doprinos nauci o enzimima – proteinskim katalizatorima, prvi put izolovanim 1878. Stvaranje novih analitičkih metoda doprinelo je formiranju biohemije kao nauke. Godine 1923. švedski hemičar Theodor Svedberg (1884-1971) dizajnirao je ultracentrifugu i razvio metodu sedimentacije za određivanje molekularne težine makromolekula, uglavnom proteina. Svedbergov asistent Arne Tiselius (1902-1971) je iste godine stvorio metodu elektroforeze, napredniju metodu odvajanja gigantskih molekula, zasnovanu na razlici u brzini migracije naelektrisanih molekula u električnom polju. Početkom 20. vijeka Ruski hemičar Mihail Semenovič Cvet (1872-1919) opisao je metodu odvajanja biljnih pigmenata propuštanjem njihove mešavine kroz cev napunjenu adsorbentom. Metoda je nazvana hromatografija. Godine 1944. engleski hemičari Archer Martin (r. 1910.) i Richard Sing (r. 1914.) predložili su novu verziju metode: zamijenili su adsorbentsku cijev filter papirom. Tako se pojavila papirna hromatografija - jedna od najčešćih analitičkih metoda u hemiji, biologiji i medicini, uz pomoć koje je krajem 1940-ih i ranih 1950-ih bilo moguće analizirati mješavine aminokiselina koje nastaju razgradnjom različitih proteina i odrediti sastav proteina. Kao rezultat mukotrpnog istraživanja, utvrđen je redoslijed aminokiselina u molekuli inzulina (Frederick Sanger, 1953), a do 1964. godine ovaj protein je sintetiziran. Sada se mnogi hormoni, lijekovi, vitamini dobivaju metodama biohemijske sinteze.
Hemija, kao jedna od nauka koja proučava prirodne pojave, nastala je u starom Egiptu prije naše ere, jednoj od tehnički najnaprednijih zemalja tog vremena. Prve informacije o hemijskim transformacijama ljudi su dobili bavljenjem raznim zanatima, kada su farbali tkanine, topili metal i pravili staklo. Tada su se pojavile određene tehnike i recepti, ali hemija još nije bila nauka. Već tada je čovječanstvu bila potrebna hemija uglavnom da bi iz prirode dobila sve materijale neophodne za život čovjeka - metale, keramiku, vapno, cement, staklo, boje, lijekove, plemenite metale itd. Od davnina, glavni zadatak hemije bio je dobivanje tvari s potrebnim svojstvima.
U starom Egiptu, hemija se smatrala božanskom naukom i njene tajne su pažljivo čuvali sveštenici. Uprkos tome, neke informacije su procurile iz zemlje i stigle u Evropu preko Vizantije.
U VIII veku, u evropskim zemljama koje su osvojili Arapi, ova nauka se proširila pod nazivom "alhemija". Treba napomenuti da u istoriji razvoja hemije kao nauke alhemija karakteriše čitavu epohu. Glavni zadatak alhemičara bio je pronaći "kamen filozofa", koji bi navodno pretvarao bilo koji metal u zlato. Unatoč opsežnom znanju stečenom kao rezultat eksperimenata, teorijski stavovi alkemičara su zaostajali nekoliko stoljeća. Ali pošto su izvodili razne eksperimente, uspjeli su napraviti nekoliko važnih praktičnih izuma. Počele su da se koriste peći, retorte, tikvice, aparati za destilaciju tečnosti. Alhemičari su pripremili najvažnije kiseline, soli i okside, opisali metode razgradnje ruda i minerala. Kao teoriju, alhemičari su koristili učenja Aristotela (384-322 pne) o četiri principa prirode (hladnoća, toplota, suvoća i vlaga) i četiri elementa (zemlja, vatra, vazduh i voda), dodajući im naknadno rastvorljivost. (sol), zapaljivost (sumpor) i metalnost (živa).
Početkom 16. veka počinje nova era u alhemiji. Njegov nastanak i razvoj povezan je sa učenjem Paracelzusa (1493-1541) i Agrikole (1494-1555). Paracelzus je tvrdio da je glavni zadatak hemije proizvodnja lekova, a ne zlata i srebra. Paracelsus je imao veliki uspjeh predloživši da se određene bolesti liječe jednostavnim neorganskim spojevima umjesto organskim ekstraktima. To je navelo mnoge doktore da se pridruže njegovoj školi i zainteresuju za hemiju, što je poslužilo kao snažan podsticaj za njen razvoj. Agricola je također studirao rudarstvo i metalurgiju. Njegovo djelo "O metalima" bilo je udžbenik o rudarstvu više od 200 godina.
U 17. veku teorija alhemije više nije ispunjavala zahteve prakse. Godine 1661. Boyle je istupio protiv ideja koje su prevladavale u hemiji i podvrgao je najstrožoj kritici teoriju alhemičara. On je prvi identifikovao centralni predmet istraživanja hemije: pokušao je da definiše hemijski element. Boyle je vjerovao da je element granica razgradnje tvari na sastavne dijelove. Razlažući prirodne supstance na njihove sastojke, istraživači su napravili mnoga važna zapažanja, otkrili nove elemente i spojeve. Hemičar je počeo da proučava šta se od čega sastoji.
Godine 1700. Stahl je razvio teoriju flogistona, prema kojoj sva tijela sposobna izgarati i oksidirati sadrže supstancu flogiston. Tokom sagorijevanja ili oksidacije, flogiston napušta tijelo, što je suština ovih procesa. Tokom skoro stoljetne dominacije teorije flogistona otkriveni su mnogi plinovi, proučavani su razni metali, oksidi i soli. Međutim, nedosljednost ove teorije ometala je dalji razvoj hemije.
Godine 1772-1777, Lavoisier je, kao rezultat svojih eksperimenata, dokazao da je proces izgaranja reakcija kombinacije kisika u zraku i goruće tvari. Tako je teorija flogistona opovrgnuta.
U 18. veku se hemija počela razvijati kao egzaktna nauka. Početkom 19. vijeka Englez J. Dalton uveo je koncept atomske težine. Svaki hemijski element dobio je svoju najvažniju karakteristiku. Atomsko-molekularna teorija postala je osnova teorijske hemije. Zahvaljujući ovom učenju, D. I. Mendeljejev je otkrio periodični zakon, nazvan po njemu, i sastavio periodni sistem elemenata. U 19. vijeku bile su jasno definisane dve glavne grane hemije: organska i neorganska. Krajem stoljeća fizička hemija se oblikovala kao samostalna grana. Rezultati hemijskih istraživanja sve više se koriste u praksi, što je dovelo do razvoja hemijske tehnologije.